Введение
Артериальная тромбоэмболия (АТЭ) — эмболизация тромба в периферической артерии, обычно острая или подострая, с тяжелыми клиническими проявлениями. У кошек риск развития АТЭ выше, чем у других видов (примерно 0,3–0,6% (1, 2)), что может быть обусловлено рядом факторов, главным образом более высокой распространенностью заболеваний миокарда и, как следствие, увеличения левого предсердия.
Значительную часть кошек c АТЭ при первичном осмотре подвергают эвтаназии, поскольку клинические проявления очень тяжелые, но у многих из тех, кто прошел лечение и пережил первоначальную стабилизацию состояния, двигательная функция в пораженных конечностях восстанавливается и сохраняется хорошее качество жизни. К сожалению, долгосрочный прогноз у кошек с АТЭ ограничен типом и тяжестью сопутствующих или вызвавших это состояние заболеваний.
У кошек склонность к образованию внутрисердечных тромбов по сравнению с другими видами животных повышена (3, 4). В большинстве случаев тромбы образуются в результате прогрессирования заболеваний сердца, приводящих к увеличению левого предсердия. Из кардиомиопатий наиболее часто встречается гипертрофическая кардиомиопатия (ГКМП), но к развитию АТЭ может привести любая кардиомиопатия или врожденный дефект (например, митральный стеноз), поражающие левые отделы сердца.
В редких случаях системную эмболизацию септическими тромбами может вызвать инфекционный эндокардит. Однако не все случаи АТЭ возникают вследствие сердечных заболеваний; наиболее распространенной некардиальной причиной АТЭ у кошек оказывается опухоль легких, осложняющаяся опухолевой эмболией (2), в некоторых случаях АТЭ может развиться спонтанно, без видимой причины.
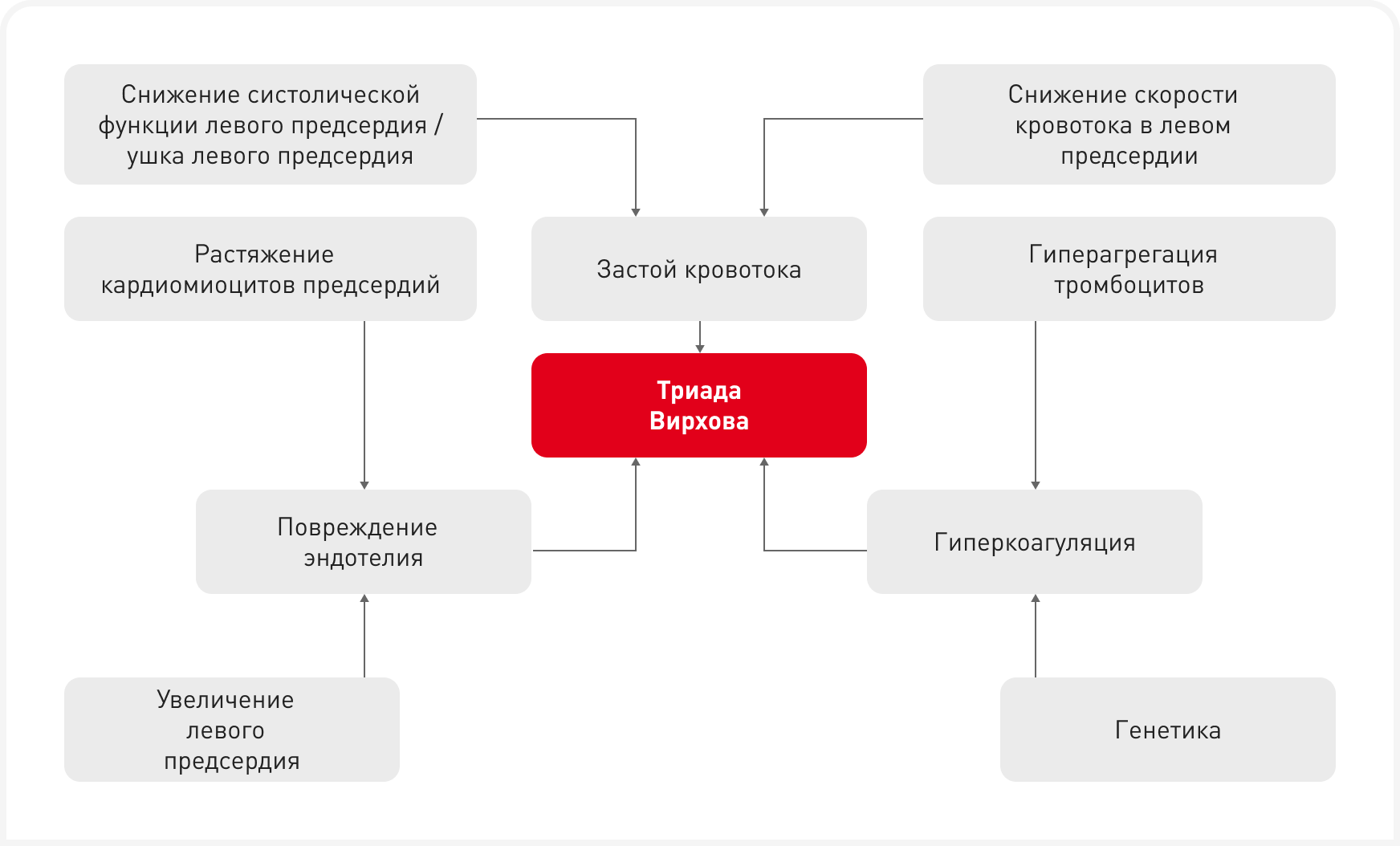
Предрасполагающие факторы к чрезмерной тромботической активности описывают триадой Вирхова: гиперкоагуляция, застой кровотока, эндотелиальная дисфункция (Рисунок 1).
К развитию АТЭ могут привести изменения в одной или нескольких точках триады, а у многих кошек с кардиогенной АТЭ, вероятно, играют роль все факторы. Одним из существенных факторов, способствующих гиперкоагуляции у кошек с АТЭ, служит гиперагрегация тромбоцитов (5, 6), но диагностировать состояние гиперкоагуляции трудно. Золотым стандартом для оценки функции тромбоцитов у кошек служит агрегометрия тромбоцитов, однако при ее выполнении очень важны квалификация и опыт оператора (5, 6).
Диапазон значений активированного частичного тромбопластинового времени (АЧТВ) и протромбинового времени (ПВ) при гиперкоагуляции и в норме может значительно перекрываться, поэтому сами по себе эти исследования только ограниченно полезны для выявления гиперкоагуляционных состояний; они лучше подходят для обнаружения гипокоагуляции.
Еще один вариант — калиброванная автоматическая тромбография; в недавних исследованиях было показано, что она более чувствительна, чем ПВ, АЧТВ и ротационная эластография (7). В будущем она может играть важную роль в измерении гемостаза у кошек. Расширение левого предсердия и/или ушка левого предсердия приводит к застою кровотока и повреждению эндотелия, и оба эти фактора могут усугубляться сопутствующей систолической дисфункцией левого предсердия.
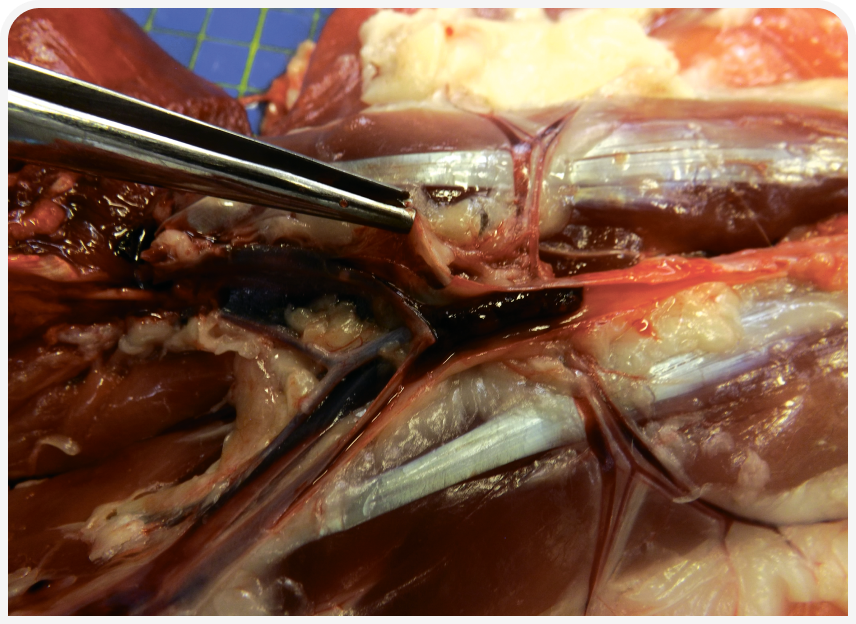
Как было отмечено ранее, первоначально тромб у большинства кошек с АТЭ образуется в левой части сердца, а затем его фрагмент либо он весь смещается. Тромб попадает в системный кровоток и в итоге застревает в артерии меньшего диаметра, чем он сам (Рисунок 2).
Образование и эмболия тромба не только непосредственно вызывают механическую обструкцию пораженной артерии, но и приводят к каскаду вазоактивных реакций, в результате чего сужаются сосуды в коллатеральной системе кровообращения. Вследствие закупорки системного кровообращения в пораженной области возникает острая ишемия тканей, снабжаемых закупоренным сосудом (сосудами), и развиваются клинические проявления АТЭ.
В большинстве случаев появляются системная гипоперфузия и шок (перераспределительный и/или кардиогенный). В нескольких исследованиях была подтверждена роль вазоактивных медиаторов в патогенезе АТЭ у кошек (8). Исследования также показывают, что введение ципрогептадина (антагониста серотонина) или высоких доз аспирина (ингибирующего тромбоксан А2) до образования тромба можно сохранить коллатеральное кровообращение и предотвратить развитие паралича (9, 10).
У котов частота случаев АТЭ выше, чем у кошек (1, 2, 11–13), вероятно, вследствие более высокой распространенности ГКМП (2, 14). Заболевание обычно развивается у животных в возрасте 8–12 лет (1, 2, 11, 12), чаще у кошек следующих пород: абиссинская, бирманская, рэгдолл (2), мейн-кун, гималайская, сиамская, персидская (1, 2, 11); однако большинство кошек с АТЭ — домашние короткошерстные или длинношерстные (1, 2, 11, 12).
АТЭ обычно дебютирует остро или подостро, практически без предупредительных симптомов. Кошки испытывают сильные страдания, что, как правило, пугает владельцев. Возникают сильная боль в пораженной конечности (конечностях), частая вокализация, явные симптомы дистресса и дискомфорта (Рисунок 3).
Клинические проявления различные, в зависимости от локализации тромбоэмбола в периферической системе кровообращения, в свою очередь, зависящей от диаметров эмбола и сосуда на различных уровнях артериального дерева. Чаще всего АТЭ у кошек поражает аппендикулярные артерии, но могут быть поражены и неаппендикулярные артерии (например, почечные, брыжеечные или мозговые сосуды).
Наиболее распространенным проявлением АТЭ у кошек служит дистальная тромбоэмболия аорты (седловой тромб) на уровне трифуркации аорты, характеризующаяся параличом или парезом одной или обеих тазовых конечностей. Если затронуты обе задние конечности, поражение может быть несимметричным.
Следующее наиболее распространенное проявление — эмболизация в пределах плечевых артерий, приводящая к снижению активности двигательных нейронов в пораженной передней конечности. В условиях общей практики у 20,8% кошек при АТЭ была поражена одна конечность, у 77,6% — две конечности, у 1,2% — три или четыре конечности (1).
В пораженных конечностях развивается явный неврологический дефицит, и кошка часто подволакивает их при ходьбе. Тяжесть клинических проявлений определяется степенью окклюзии сосудов, при этом частичная окклюзия приводит к появлению менее выраженных признаков.
В зависимости от локализации эмболии могут наблюдаться другие симптомы (включая нарушения со стороны центральной нервной системы, рвоту или боль в животе) (2), и при поражении неаппендикулярных артерий диагностика может оказаться сложной. Обычно развивается гипотермия, в первую очередь в результате системной гипоперфузии и шока вследствие каскада вазоактивных реакций при ишемии тканей; также может иметь дополнительное значение закупорка артериального кровоснабжения задних конечностей.
В некоторых случаях АТЭ у кошек могут быть выявлены признаки основного заболевания сердца (например, шумы в сердце, ритм галопа или аритмия), но отсутствие аускультативных нарушений не исключает заболевания сердца. Ритм галопа свидетельствует о неблагоприятном прогнозе (14).
У некоторых кошек также могут проявляться признаки сопутствующей застойной сердечной недостаточности (ЗСН), включая тахипноэ, одышку, ортопноэ, хрипы в легких и дыхание через открытый рот. В 40–67% случаев АТЭ сочетается с ЗСН (2, 12, 13), но дыхание через открытый рот и тахипноэ также могут быть обусловлены болью. Острые проявления АТЭ часто оказываются первыми признаками тяжелого поражения сердца, при этом у большинства кошек до развития АТЭ сердечных заболеваний в анамнезе не отмечали.
Обычно обнаруживают стрессовую гипергликемию (из-за выброса адреналина и кортизола), часто — преренальную или ренальную азотемию, при этом уровни азота мочевины в крови (АМК) повышаются чаще и, как правило, более серьезно, чем уровни креатинина (2, 11). Преренальная азотемия обусловлена плохой системной перфузией и шоком; может быть повышено соотношение АМК:креатинин.
Ренальная азотемия возникает непосредственно вследствие тромбоэмболии почечной артерии (хотя в некоторых случаях определенную роль также могут играть острое повреждение почек вследствие шока или существующая хроническая болезнь почек). Ишемия мышц приводит к выраженному повышению уровня креатинкиназы в сыворотке крови; также часто наблюдается гиперфосфатемия.
Одним из наиболее значительных и потенциально опасных для жизни осложнений АТЭ у кошек является гиперкалиемия, которая может быть тяжелой и часто вызвана реперфузионным повреждением после восстановления перфузии тканей, хотя в некоторых случаях наблюдается и при первичном осмотре. Также могут отмечаться другие электролитные нарушения, такие как гипокальциемия и гипонатриемия. Могут быть повышены уровни D-димеров, но, как отмечалось выше, обычные анализы свертываемости крови (такие как ПВ и АЧТВ) часто остаются в пределах нормального диапазона.
Аппендикулярную АТЭ обычно можно диагностировать уже при непосредственном осмотре, путем выявления пяти главных симптомов: боль, паралич/парез, отсутствие пульса, бледность, пойкилотермия (Рисунок 4).
При первичном осмотре пораженные конечности болезненны, часто с ригидными мышцами, признаками снижения активности двигательных нейронов от легкого пареза до полного паралича.
В одном исследовании было показано, что некоторая двигательная функция сохранялась в пораженных конечностях примерно у 34% кошек, а при АТЭ в передних конечностях или в одной задней конечности вероятность сохранения двигательной функции была выше (2).
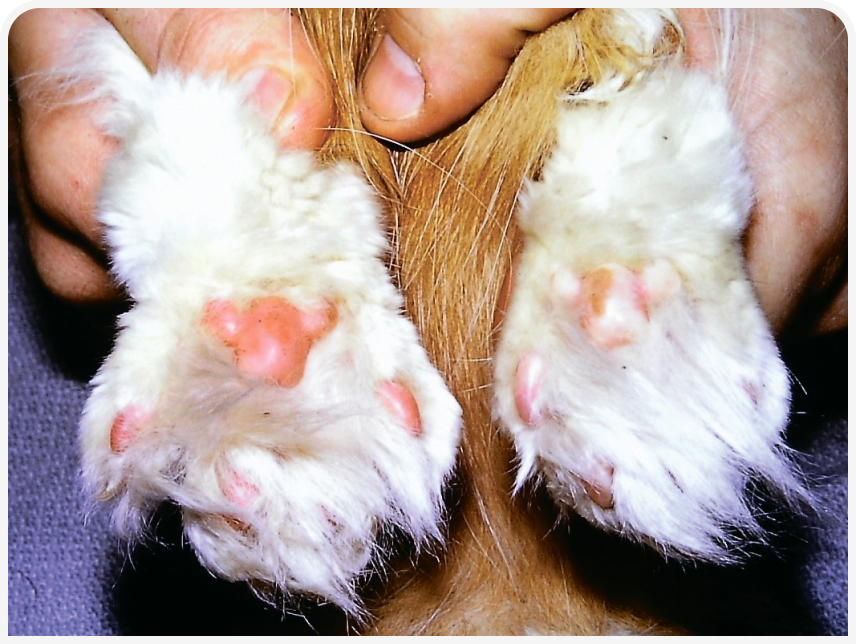
В большинстве случаев артериальные импульсы дистальнее уровня эмболии отсутствуют или очень слабые, но следует помнить, что иногда у кошек в отсутствие АТЭ трудно определить пульс, особенно на передних конечностях; также его сложно обнаружить у пациентов с ожирением или неконтактных, особенно на фоне острой боли. Диагностику облегчает доплеровское исследование пораженной конечности(ей). Также следует осмотреть подушечки лап и когтевые ложа пораженных конечностей; они обычно бледные или даже цианотичные, в зависимости от степени ишемии тканей. Полезно сравнить их с непораженными конечностями (Рисунок 5).
Пойкилотермия (т. е. более низкая температура в пораженных конечностях по сравнению с непораженными) обусловлена уменьшением или отсутствием кровотока дистальнее места эмболии. Было показано, что разница в температуре на 2,4° C между ипсилатеральными пораженными и непораженными конечностями при инфракрасной термографии у кошек высокоспецифична (100%) и высокочувствительна (80%) для диагностики АТЭ (15).
Дополнительные подтверждающие данные можно получить, измерив и сравнив уровни глюкозы крови и сывороточного лактата в пораженных и непораженных конечностях. В образцах крови из периферических вен пораженных конечностей дистальнее места эмболии по сравнению с образцами из центральных вен или непораженных конечностей уровни глюкозы ниже, а лактата выше; показано, что разница абсолютной концентрации глюкозы в крови ≥ 30 мг/дл между образцами из центральных и периферических сосудов позволяет выявлять АТЭ у кошек со 100%-ной чувствительностью и 90%-ной специфичностью (16).
Оптимальные пороговые значения для диагностики АТЭ у кошек по разнице в концентрации лактата в сыворотке крови между пораженными и непораженными конечностями не определены. Для постановки диагноза или определения причины развития АТЭ применяют ряд методов диагностической визуализации (ультразвуковое исследование, ангиография, компьютерная томография или магнитно-резонансная томография пораженной артерии), но необходимость в них возникает редко.
Стабилизация острого состояния и лечение в раннем периоде
Поскольку большинство кошек испытывают при АТЭ сильную боль и дистресс, при начальной терапии следует прежде всего быстро и эффективно обезболить кошку, в идеале полными агонистами мю-рецепторов опиоидов (например, метадон, фентанил, оксиморфон или гидроморфон). Во всех случаях дыхательной недостаточности показана терапия кислородом (Рисунок 6).
При принятии решения о том, продолжать лечение или провести эвтаназию, следует откровенно обсудить с владельцами прогноз. Ректальная температура ниже 37° C (1, 2), брадикардия (2, 11), отсутствие двигательной функции (2), поражение более чем одной конечности (2) и подтвержденная сопутствующая ЗСН сопровождаются снижением выживаемости.
После первоначальной стабилизации состояния пациента с помощью анальгезии и кислородной терапии и при отсутствии риска нарушения стабильности состояния пациента проводят обследование на наличие признаков ЗСН.
Отек легких выявляют с помощью рентгенографии, плевральный выпот — посредством «прикроватного» УЗИ (POCUS). При значительном плевральном выпоте проводят торакоцентез. Кошкам с подтвержденной ЗСН (или при высокой степени подозрения на ЗСН) назначают диуретическую терапию (фуросемид в дозе 1–2 мг/кг внутривенно или внутримышечно) и повторяют ее через соответствующие интервалы до достижения эффекта. Затем интервал дозирования по необходимости корректируют.
Следует незамедлительно устранить признаки нарушения системной перфузии и шока, развивающиеся в большинстве случаев АТЭ. При тяжелой декомпенсированной сердечной недостаточности может возникнуть кардиогенный шок, причем ишемия тканей и высвобождение вазоактивных веществ могут привести к развитию перераспределительного шока; метод купирования гипоперфузии выбирают в зависимости от характера шока, но при первичном осмотре различить их трудно.
При обезвоживании без признаков ЗСН можно рассмотреть проведение инфузионной терапии, но при внутривенном введении жидкостей животным с сопутствующими заболеваниями сердца следует соблюдать осторожность. Поэтому кошкам с декомпенсированной сердечной недостаточностью и ЗСН, особенно с признаками систолической дисфункции миокарда, может быть более полезно назначение препаратов с положительным инотропным действием, например пимобендана (0,15 мг/кг внутривенно или 0,3 мг/кг внутрь); однако данных за улучшение общей выживаемости при применении таких препаратов нет.
Слабая системная перфузия и шок во многих случаях приводят к снижению ректальной температуры и даже развитию общей гипотермии, но активного согревания следует избегать, пока не будет скорректирована системная перфузия, поскольку такое согревание только ухудшит общую перфузию, приведет к расширению периферических сосудов с увеличением оттока крови от жизненно важных органов и тем самым усугубит клинические последствия шока.
После стабилизации состояния пациента следует начать антитромботическую терапию, чтобы предотвратить распространение существующих и образование новых тромбов, но эти препараты не лизируют существующие тромбы. Рекомендуются низкомолекулярный гепарин, такой как дальтепарин (по 75–150 ед/кг подкожно каждые 6 ч) (17), либо нефракционированный гепарин (по 250–300 ед/кг каждые 6 ч) (17,18), введение которых обычно прекращают через 2–3 дня после стабилизации состояния и перевода пациента на пероральные антитромботические препараты.
Как только пациент сможет переносить пероральные препараты, следует начать прием клопидогрела. Этот препарат — антагонист аденозиндифосфата, обратимо ингибирующий агрегацию тромбоцитов. Рекомендуется начальная нагрузочная доза 75 мг внутрь каждые 24 ч, затем поддерживающая доза 18,75 мг внутрь каждые 24 ч (19). У многих кошек возникает отвращение к клопидогрелу, поскольку он горчит, и следует рассмотреть варианты его приема, например, в желатиновых капсулах или жидкости с приятным вкусом.
В остальном клопидогрел обычно переносится хорошо, хотя при более высокой дозировке может увеличиваться кровоточивость (например, появляются кровоподтеки). У пациентов на этой терапии кровь следует брать из периферических вен, а гемостаз после венопункции обеспечивать соответствующими компрессионными повязками.
Клопидогрел более эффективен для вторичной профилактики АТЭ, чем аспирин (20), но, поскольку механизмы действия этих препаратов различаются, у некоторых пациентов можно рассмотреть проведение двойной терапии, хотя эффективность этой комбинации не исследована. Аспирин подавляет агрегацию тромбоцитов путем необратимого ингибирования образования тромбоксана А2 на тромбоцитах, и обычно его назначают в дозе 20,25–81 мг на кошку каждые 72 часа. Аспирин назначают только после возобновления приема пищи, чтобы снизить риск образования язв в желудочно-кишечном тракте.
Тромболитическая терапия, включая тканевой активатор плазминогена (21, 22), стрептокиназу (11) и урокиназу (23), у кошек с АТЭ не рекомендуется; при применении этих препаратов не выявлено улучшения выживаемости по сравнению со стандартной антитромботической терапией, кроме того, развивались значимые осложнения, в частности опасная для жизни гиперкалиемия, скорее всего, в рамках реперфузионного повреждения.
У пациента следует регулярно оценивать уровень боли и проводить эффективную анальгезию на протяжении как минимум 24–48 часов. После этого срока потребность в полных агонистах опиоидных мю-рецепторов значительно уменьшается, и может быть достаточно бупренорфина (частичного агониста мю-рецепторов опиоидов). Кроме того, после стабилизации состояния пациента следует провести дальнейшую диагностику для изучения возможных причин АТЭ. Получают гемограмму, биохимический анализ сыворотки крови, порводят эхокардиографию или ультразвуковое исследование всех артерий, поражение которых выявлено при первоначальном обследовании.
Реперфузионное повреждение ишемизированных тканей может привести к развитию тяжелой угрожающей жизни гиперкалиемии и ацидоза и является одним из наиболее значимых осложнений терапии АТЭ. Всех пациентов следует тщательно наблюдать для выявления биохимических нарушений, особенно в первые 48–72 часа после появления симптомов.
При необходимости реперфузионное повреждение следует незамедлительно устранить соответствующей терапией (например, введением декстрозы, инсулина с декстрозой, глюконата кальция, бикарбоната натрия). Манипуляций с пораженными конечностями (включая физиотерапию) следует избегать по крайней мере в течение 72 часов, поскольку они могут вызвать острый приток калия и лактата в кровоток, увеличивая риск реперфузионного повреждения.
Длительное лечение
Клопидогрел (18,75 мг/кошка) следует принимать длительно, поскольку показано, что при вторичной профилактике АТЭ он более эффективен, чем аспирин (20). Пероральные ингибиторы фактора Ха (например, ривароксабан в дозе 0,5–1 мг/кг/сут) предложены в качестве альтернативной антитромботической терапии как для краткосрочного, так и для долгосрочного лечения АТЭ, но перспективные данные об их эффективности ограничены.
Однако клинические исследования ривароксабана продолжаются, и при ретроспективном анализе двойной терапии с использованием клопидогрела и ривароксабана было показано, что эта комбинация хорошо переносится и вызывает небольшое количество нежелательных эффектов (24). В настоящее время такие препараты рекомендуется назначать в комбинации со стандартной терапией клопидогрелом, а не в качестве замены ей (19).
Терапию низкомолекулярным гепарином или нефракционированным гепарином можно длительно проводить в домашних условиях кошкам после тяжелой АТЭ или при рецидивирующей АТЭ, но для долгосрочного лечения эти варианты лечения используют редко, и данных об их эффективности недостаточно.
В большинстве случаев АТЭ из‑за высокой распространенности заболеваний сердца необходима соответствующая терапия клинических проявлений сердечных заболеваний. При сопутствующей ЗСН требуется постоянная диуретическая терапия фуросемидом (по 0,5–2 мг/кг перорально каждые 8–12 часов). Следует оценить функцию почек и уровень электролитов и, если они в норме, рассмотреть возможность применения ингибиторов ангиотензинпревращающего фермента (АПФ) (беназеприл в дозе 0,5–1 мг/кг либо эналаприл в дозе 0,25–0,5 мг/кг, оба перорально, каждые 12–24 часов) с последующим тщательным мониторированием функции почек.
У кошек с азотемией или заболеванием почек требуется соблюдать осторожность. Кошкам с признаками систолической дисфункции можно назначать безрецептурный препарат пимобендан (0,3 мг/ кг перорально каждые 12 часов). Антиаритмическую терапию определяют исходя из типов и тяжести сопутствующих аритмий; углубленный обзор долгосрочного ведения таких случаев приведен по ссылке (19).
Физиотерапию, включая упражнения на пассивную подвижность пораженных конечностей, рекомендуется начинать сразу после стабилизации состояния пациента, хорошего контроля боли и уменьшения риска реперфузионного повреждения. Владельцев обучают выполнению упражнений; пассивные манипуляции с пораженными конечностями следует продолжать дома по крайней мере несколько недель, пока двигательная функция не улучшится и не уменьшится риск развития контрактуры мышц.
В одном исследовании кошек с диагностированной АТЭ в общей практике было показано, что как минимум через 7 дней после первичного осмотра были живы только 12% кошек (1); 61,2% были подвергнуты эвтаназии при первичном осмотре, 8,8% были подвергнуты эвтаназии и 2,8% умерли в течение 24 часов после начала лечения, а в целом после 24 часов выжили только 27,2% (1).
Напротив, в условиях направляющего учреждения была описана выживаемость около 30–40% (и даже до 73%) (2, 11–13), хотя в качестве объяснения этих цифр нельзя исключить влияние систематической ошибки при направлении пациентов.
Низкие показатели общей выживаемости в общей ветеринарной практике могут, наоборот, отражать восприятие прогноза как безнадежного и изначальное предубеждение, что при первичном осмотре следует проводить эвтаназию больных кошек. Более того, выживаемость кошек с только одной пораженной конечностью может достигать 70–80% (11, 13) и даже 90%, если при первичном осмотре сохраняется некоторая двигательная функция (12).
Клинические проявления АТЭ часто значительно улучшаются после первых 24–48 часов терапии, и у многих пациентов, выживших дольше 48–72 часов, некоторые или даже все двигательные функции восстанавливаются в течение 1–2 месяцев. Такие результаты свидетельствуют, что терапия в первые 72 часа оправдана и потенциально может увеличить общую выживаемость.
Однако значимыми негативными прогностическими показателями служат две или более пораженные конечности (1, 2), предшествующие АТЭ в анамнезе (14), брадикардия (2, 11), сердечный ритм галопа (14) и ректальная температура ниже 37 °C (1, 2); причем ректальная температура ниже 37,2 °C при первичном осмотре сопровождается выживаемостью ниже 50% (2).
У кошек, переживших АТЭ, также могут наблюдаться долгосрочные осложнения. Частоту развития мышечных контрактур можно уменьшить с помощью физиотерапии во время госпитализации и продолжения ее дома после выписки. Развившаяся при АТЭ ишемия может вызывать на пораженных конечностях вторичные некроз и шелушение кожи, причем иногда через несколько дней.
Такие повреждения могут ограничиваться отдельными пальцами или поражать большие участки кожи и требовать хирургического лечения. Если перфузия настолько плохая, что приводит к некрозу всей конечности, может потребоваться ее ампутация (2). Стойкий неврологический дефицит может осложняться экскориациями из‑за подволакивания конечностей и самоповреждением пораженных конечностей из‑за нейропатической боли.
Для лечения нейропатической боли у таких кошек можно рассмотреть терапию габапентином, но ее эффективность при АТЭ не изучена. Риски и предупреждающие симптомы этих осложнений следует четко объяснить владельцам, в идеале еще до принятия любых решений о начале терапии или эвтаназии.
Как и при многих других заболеваниях, профилактика лучше лечения, но, несмотря на это, исследований эффективности первичной профилактики (т. е. предотвращения первого события АТЭ у пациента из группы риска) нет. В настоящее время кошкам из группы риска для профилактики АТЭ рекомендуется назначать клопидогрел (19), и показано, что у кошек после первоначального события АТЭ он эффективнее аспирина увеличивает период до развития рецидива АТЭ или сердечной смерти (20).
Наиболее значительным препятствием для профилактики, вероятно, является выявление кошек из группы риска, поскольку субклинические заболевания сердца, о которых владельцы могут не знать, широко распространены, поэтому при обнаружении у бессимптомных кошек шума, ритма галопа или аритмии следует провести обследование на наличие заболевания сердца. С повышенным риском развития АТЭ у кошек с известными заболеваниями сердца связан ряд эхокардиографических параметров.
К ним относятся наличие спонтанного эхо-контраста («дым») (Рисунок 7), увеличение левого предсердия от умеренной до тяжелой степени, снижение скорости движения по ушку левого предсердия, уменьшение фракционного укорочения предсердий, уменьшение фракции выброса из левого предсердия и увеличение толщины стенки левого желудочка; все эти признаки у кошек считают показаниями для начала терапии клопидогрелом при бессимптомном течении заболевания.
В недавно предложенных рекомендациях кардиомиопатию стадии В2 (бессимптомную с увеличением левого предсердия от умеренной до тяжелой степени) считают повышающей риск развития ЗСН или АТЭ и рекомендуют у всех кошек на этой или более высокой стадии применять клопидогрел (19).
Эффективность профилактики АТЭ при двойной терапии клопидогрелом и аспирином либо ингибитором фактора Ха по сравнению с терапией только клопидогрелом в настоящее время неизвестна. Большинство стратегий профилактики направлены на факторы, связанные с кардиогенной АТЭ, поэтому рекомендаций для кошек с некардиогенными причинами или без идентифицируемой причины АТЭ в настоящее время недостаточно.
Хотя артериальная тромбоэмболия (АТЭ) у кошек может проявляться остро и внезапно, а долгосрочный прогноз обычно осторожный или неблагоприятный, это ни в коем случае не смертный приговор. При быстром проведении вмешательства, осторожных клинических решениях и интенсивной терапии общий прогноз вариабельный и зависит от причины и тяжести проявляющихся признаков.
Многие клинические проявления купируются в течение первых 72 часов после развития АТЭ, поэтому во многих случаях целесообразно проводить терапию по крайней мере в течение этого начального периода. Этиология и патофизиология
Клинические проявления
.png)
Диагностические данные
.png)
.png)
Лечение и исход

Прогноз
Профилактические мероприятия
.png)
Заключение
«Артериальная тромбоэмболия у кошек »!
баллы


были начислены ранее


телефона ниже для сброса пароля.



на номер
+7 {{ formatted_phone }}


Вы успешно прошли тест!
зарегистрироваться/авторизоваться
способ авторизации/регистрации.
{{ formatted_phone }}.
Введите последние четыре цифры номера входящего звонка.

весь модуль
всех видеоуроков модуля














 272
272  10 мин
10 мин







