Введение
Кальций — пятый по распространенности элемент в организме, в виде незаменимого катиона содержащийся в составе биологических жидкостей и клеточных органелл. Он обеспечивает многие жизненно важные внутриклеточные и внеклеточные функции, включая нервно-мышечную передачу, ферментативные реакции, свертывание крови, вазомоторный тонус, секрецию гормонов и метаболизм костной ткани.
Кальций широко распределен в клеточных тканях, поэтому быстрые колебания его внутриклеточных концентраций после активации рецепторов плазматической мембраны оказывают на внутриклеточные реакции регулирующее воздействие, а также передают в клетку внешние сигналы для управления внутриклеточными биологическими функциями (1).
Внутриклеточный кальций играет ключевую роль в нормальной жизнедеятельности клеток, но возможности измерения содержания кальция в клинических условиях ограничены его выявлением в биологических жидкостях, где он существует в трех различных формах: ионизированной, связанной с белками и в комплексе с анионами или органическими кислотами.
Биологически активна ионизированная форма кальция (iCa), проходящая через плазматические мембраны по специфичным ионным каналам и с помощью активных переносчиков и катионообменников (2) и составляющая 50% от общего содержания кальция в сыворотке крови. Оставшаяся фракция распределяется приблизительно как 40% связанной с белком и 10% в составе комплексов.
Учитывая важность iCa для клеточных функций, организм должен для обеспечения надлежащей физиологической активности множества клеточных, тканевых и органных систем строго регулировать его концентрацию; для этого организм согласует действие паратиреоидного гормона (ПТГ), 1,25-дигидроксихолекальциферола (активной формы витамина D3, или кальцитриола) и кальцитонина (3). Аналогично значению для внутриклеточной передачи сигналов, уровень кальция во внеклеточной жидкости также регулирует клеточные функции во многих жизненно важных железистых и эпителиальных тканях, включая паращитовидную железу, С-клетки щитовидной железы и почки.
Гомеостаз кальция
Организм выравнивает концентрации кальция путем взаимодополняющих и/или синергетических биологических воздействий на три органа-мишени, а именно: на почки, тонкий кишечник и неорганический костный матрикс (гидроксиапатит), тремя основными медиаторами: ПТГ, кальцитонином и кальцитриолом (3) (Рисунок 1).
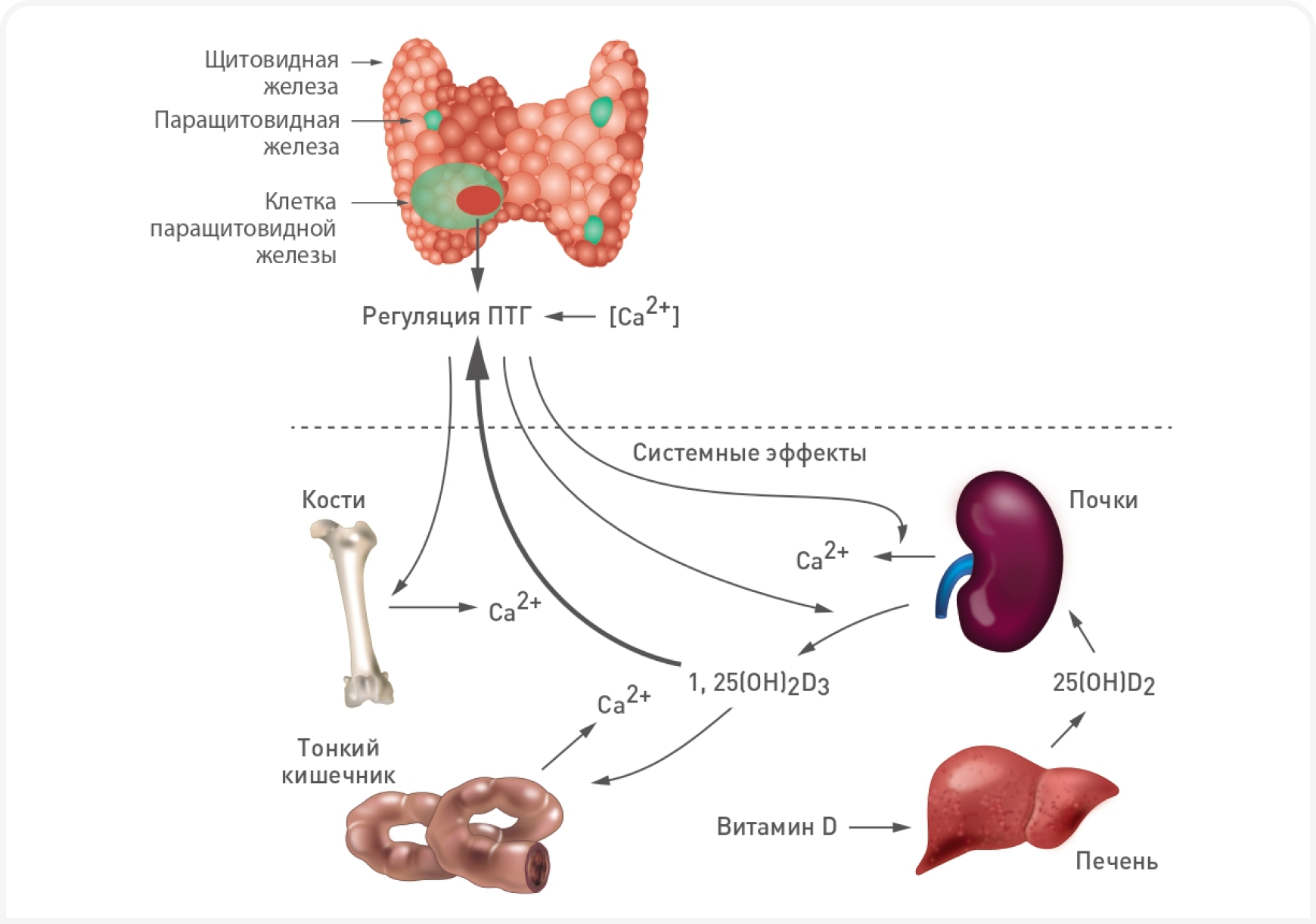
ПТГ — основной регулятор, ежеминутно выравнивающий колебания уровня кальция в организме. Если уровень кальция повышен, секреция ПТГ снижается, вызывая выведение кальция из организма через дистальные канальцы почек, снижая всасывание кальция в кишечнике и уменьшая резорбцию кости остеокластами (4).
Напротив, если уровень кальция в сыворотке крови снижен, паращитовидные железы выделяют ПТГ, который вызывает реабсорбцию кальция и выведение фосфора в дистальных канальцах почек. ПТГ также косвенно способствует всасыванию кальция в тонком кишечнике, повышая в проксимальных почечных канальцах активность 1-альфа-гидроксилазы и тем самым стимулируя превращение витамина D в высокоактивный витамин D3 (кальцитриол) (4).
Кроме того, ПТГ воздействует на скелетную ткань, стимулируя пролиферацию существующих костеобразующих клеток (остеобластов), что быстро приводит к повышению минеральной плотности костной ткани (5). Однако хроническая активация ПТГ может усиливать экспрессию RANKL остеобластами, которая активирует остеокласты и увеличивает продолжительность их жизни, что приводит к усилению резорбции костной ткани (6).
Кальцитриол участвует в регуляции кальция, главным образом активируя синтез белков кальбиндина-D, увеличивающих всасывание кальция в тонком кишечнике и тем самым — его поступление в кровоток (7). Кальцитриол также может по механизму отрицательной обратной связи превращаться в менее активный метаболит 24,25-дигидроксихолекальциферол, а также снижать уровень кальция путем снижения транскрипции мРНК белка ПТГ.
Кальцитонин не играет большой роли в ежеминутной регуляции уровня кальция, но при быстром повышении уровня кальция в сыворотке крови экстренно его снижает. Кальцитонин высвобождается С-клетками щитовидной железы при стимуляции гиперкальциемией и при употреблении пищи с высоким содержанием кальция, вызывающей секрецию кишечных гормонов (например, гастрина и холецистокинина), и его биологическая активность в основном опосредуется ингибированием остеокластической резорбции костной ткани (8).
Гомеостаз кальция
Гиперкальциемия и у собак, и у кошек сопровождается рядом физиологических и патологических проявлений, которые можно в широком смысле классифицировать на зависящие и не зависящие от паращитовидных желез. Зависящие от паращитовидных желез причины включают первичный гиперпаратиреоз и (в редких случаях) вторичный пищевой или почечный гиперпаратиреоз.
Все остальные причины гиперкальциемии считают не зависящими от паращитовидных желез: онкологические (Рисунки 2 и 3), токсические, идиопатические, метаболические, костные и гранулематозные заболевания (9). В недавних исследованиях на большом количестве животных-компаньонов оценивали наиболее частые патологические причины ионизированной гиперкальциемии.
У собак это были опухоли, первичный гиперпаратиреоз и гипоадренокортицизм.
Для сравнения, у кошек наиболее частыми причинами были опухоли (например, плоскоклеточный рак полости рта), хронические заболевания почек, идиопатическая гиперкальциемия вторичная на фоне нарушения кальций-чувствительного аппарата (рецепторов) и (реже) гипервитаминоз D (10–14).
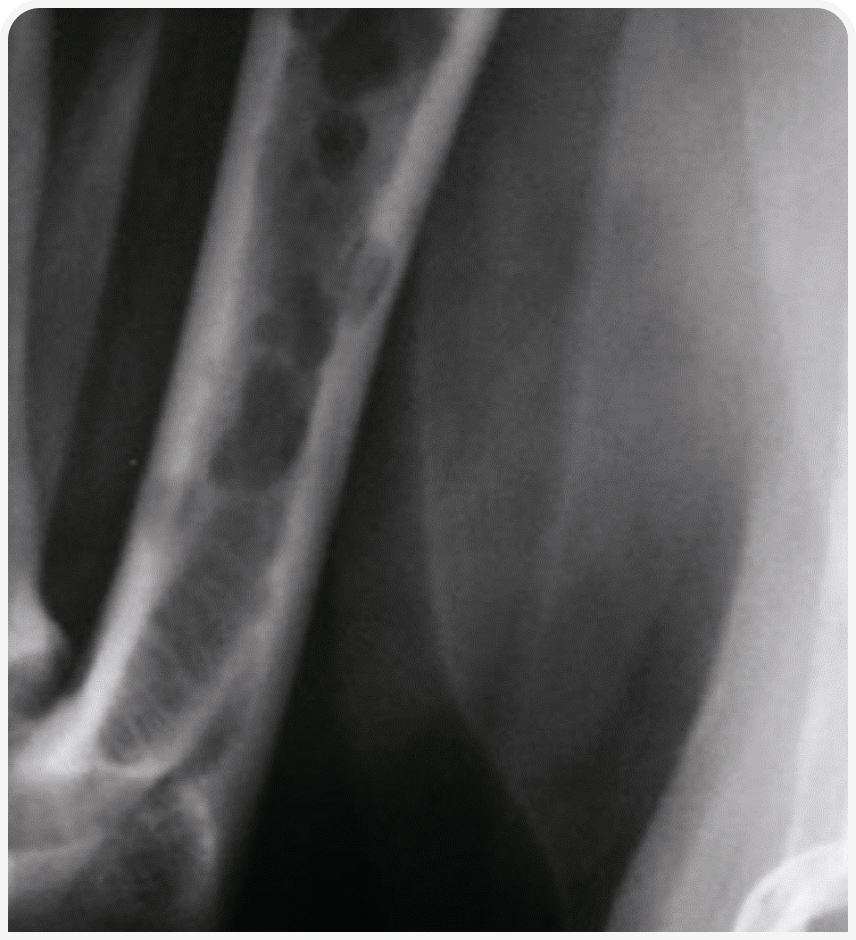
В целом наиболее частой причиной гиперкальциемии у животных-компаньонов оказывается рак: связанную с раком гиперкальциемию выявляют примерно у 60% собак (и 30% кошек) (11–13) (Рисунки 4 и 5).
Гиперкальциемия может развиваться при ряде серьезных заболеваний. По-английски их список очень удачно описывается мнемоником GOSH DARN IT, означающим восклицание «Черт возьми!» (Таблица 1).
При раке повышение уровня кальция встречается часто и может быть вызвано несколькими механизмами (15, 16).
Первая и наиболее частая причина гиперкальциемии — выработка растворимых факторов опухолевыми клетками, приводящая к резорбции кости, так называемой гуморальной гиперкальциемии злокачественных опухолей (humoral hypercalcemia of malignancy — HHM).
.png)
.png)
.png)
Второй механизм — непосредственное внедрение опухолевых клеток в кость, приводящее к остеолизу, обычно наблюдающемуся при карциномах или злокачественных новообразованиях кроветворного костного мозга, таких как лейкозы, лимфома, миелома. Наконец, и реже всего, выработка активной формы витамина D клетками, экспрессирующими 1-α-гидроксилазу, усиливает всасывание кальция в кишечнике.

Гуморальная гиперкальциемия злокачественных опухолей (humoral hypercalcemia of malignancy — HHM)
Гуморальная гиперкальциемия злокачественных опухолей может сопровождаться злокачественной секрецией белка, связанного с паратиреоидным гормоном (parathyroid hormone-related peptide — PTHrP), структурно подобного ПТГ (17), и цитокинов, таких как IL-1, IL-6 или фактор некроза опухоли (15).
Эти гуморальные факторы приводят к генерализованной и диффузной остеокластической резорбции, при рентгенографии не проявляющейся поражениями костей. Поскольку PTHrP — секретируемый белок, чрезмерное количество этого гормона может выделяться любыми секреторными клетками, подвергшимися злокачественной трансформации.
Чаще всего HHM бывает вызвана лимфомой (LSA), особенно лимфомой средостения; у собак (и кошек) гиперкальциемию также вызывают другие опухоли: аденокарцинома апокриновой железы анального мешка (apocrine gland anal sac adenocarcinoma — AGASACA), рак щитовидной железы, миелома, опухоли с поражением большого количества костей, тимома, плоскоклеточный рак, рак молочной железы/аденокарцинома, меланома, первичная опухоль легкого, хронический лимфолейкоз, ангиомиксома почек, опухоли паращитовидной железы. Как правило, гиперкальциемия развивается у 10–35% собак с LSA, у более чем 25% собак с AGASACA и примерно у 20% собак с миеломой.
Клинические проявления
Учитывая широкий спектр физиологических функций ионов кальция, и гиперкальциемия, и гипокальциемия вызывают полисистемные эффекты (10, 11). Повышенная концентрация кальция в сыворотке крови подавляет функции клеток, изменяя проницаемость клеточных мембран и активность клеточных мембранных насосов.
Увеличение внутриклеточного содержания iCa может нарушать клеточные функции и снижать в клетках выработку энергии, что может привести к их гибели и к развитию дистрофической и/или метастатической минерализации. Гиперкальциемия может поражать многие ткани, но клинически наиболее значимо воздействует на центральную нервную систему, желудочно-кишечный тракт, сердце, почки.
Независимо от причины гиперкальциемии, ее клинически значимым следствием является нарушение функции почек, особенно при новообразованиях (18). Клинические признаки гиперкальциемии могут быть неспецифичными, скрытыми и различаться по тяжести, но чаще всего включают первичную полиурию с компенсаторной полидипсией (ПУПД), анорексию, летаргию, слабость, рвоту, подавленность, подергивания мышц, аритмии, судороги (9). У кошек гиперкальциемия чаще проявляется симптомами со стороны желудочно-кишечного тракта, особенно анорексией и рвотой (19).
Диагностическое обследование при гиперкальциемии
У животных-компаньонов точность измерения уровня кальция выше при определении iCa, чем общего содержания кальция. Интересно, что концентрация кальция, как правило, больше, чем при других причинах, повышается при гиперкальциемии злокачественных опухолей (12, 13).
Обследование при подозрении на гиперкальциемию начинают с подробного сбора анамнеза и непосредственного обследования, включая тщательную оценку состояния периферических лимфатических узлов и пальпацию прямой кишки (для исключения AGASACA) (Рисунки 6–8).
.png)
.png)
На основании результатов можно провести дополнительные диагностические исследования (включая общий анализ крови, биохимический анализ крови, анализ мочи, рентгенографию органов грудной клетки, УЗИ органов брюшной полости), чтобы подтвердить клинические подозрения или, наоборот, обнаружить заболевания, не выявленные при непосредственном обследовании.
Если после этих диагностических мероприятий выявить основную причину гиперкальциемии не удается, можно провести дополнительные исследования, включая измерение концентраций ПТГ, PTHrP и кальцитриола в сыворотке крови.
При гиперкальциемии злокачественных опухолей концентрация ПТГ в сыворотке крови должна быть низкой или неопределяемой, а уровни PTHrP в сыворотке крови могут быть измеримыми и/или повышенными.
Уровень кальцитриола в сыворотке крови обычно находится в пределах нормы, но может быть повышен или снижен.
Уровень кальцитриола в сыворотке крови обычно находится в пределах нормы, но может быть повышен или снижен.
.png)
Помимо этих традиционных диагностических мероприятий, если причина нарушения не выявлена, можно рассмотреть проведение дополнительных исследований: рентгенографии костей, сканирования костей (ядерная сцинтиграфия), аспирации костного мозга, компьютерной томографии (КТ) (Рисунки 9–11).
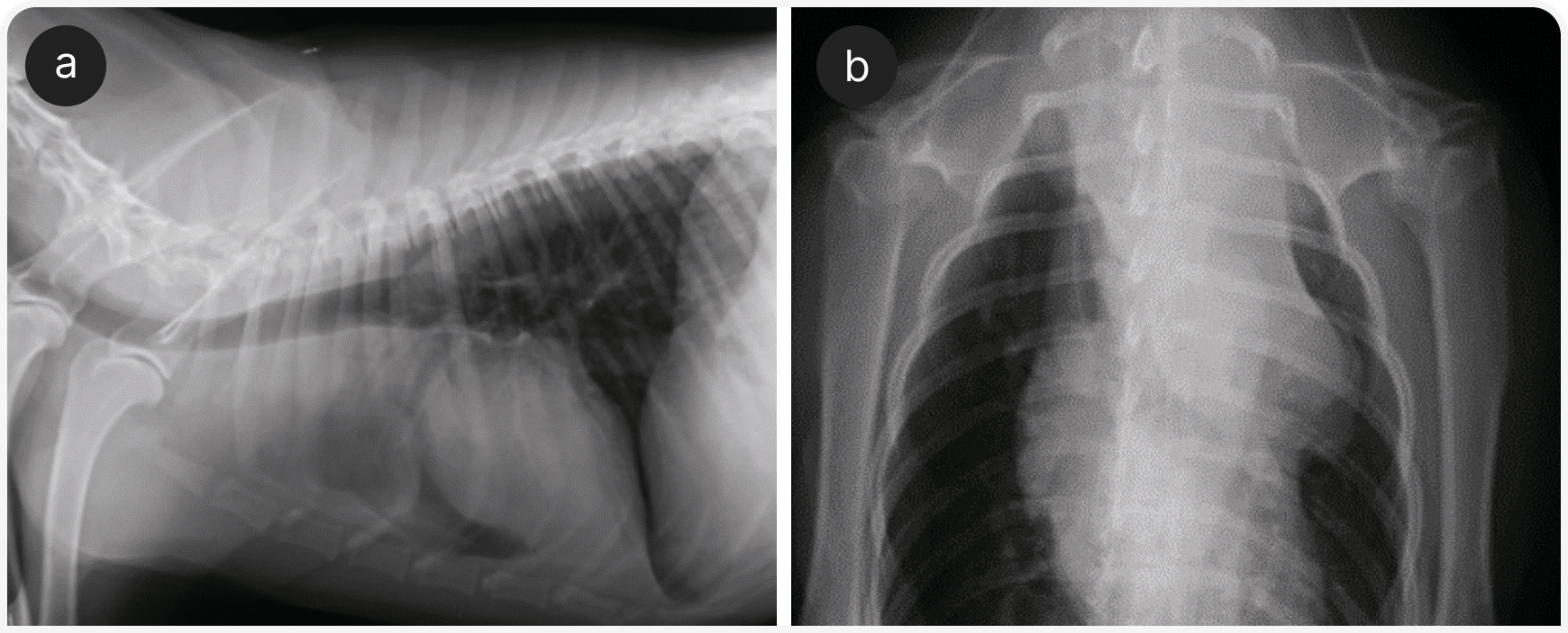
Нарушения кальциевого обмена могут возникать при ряде серьезных и угрожающих жизни состояний, причем без лечения гиперкальциемия может сама по себе, независимо от причины, привести к сокращающим жизнь пациента осложнениям (20).
Для измерения уровня iCa требуются специализированные анализаторы, не всегда доступные в ветеринарной медицине. Поэтому клиницистам часто приходится ограничиваться оценкой общего содержания кальция (tCa), включающего все три фракции кальция в сыворотке крови.
К сожалению, точно интерпретировать показатель общего содержания кальция может быть сложно, поскольку у отдельных пациентов он не отражает статуса iCa. Предложен ряд корректирующих формул на основании уровней альбумина и общего белка, однако они ненадежны и, по данным исследований, не позволяют подтвердить и скорректировать наблюдаемое несоответствие диагностического значения общего содержания кальция и iCa (20, 21).
В связи с этим рекомендуется при любых нарушениях общего содержания кальция дополнительно проводить непосредственное диагностическое количественное определение истинных концентраций iCa.
.png)
.png)
Лечение
Учитывая широкий спектр причин гиперкальциемии, необходимое лечение, тяжесть клинических проявлений и общий прогноз определяются ее этиопатогенезом. Единого протокола лечения, неизменно эффективного при любых причинах гиперкальциемии, не существует, но в большинстве случаев немедленный клинический эффект можно обеспечить индукцией кальциуреза.
Чтобы подобрать оптимальное лечение гиперкальциемии, выявляют и лечат ее основную причину, хотя точно идентифицировать некоторые патологические процессы может быть сложно и труднодостижимо. Степень агрессивности лечения в конечном счете подбирают, исходя из клинического статуса пациента.
Для лечения гиперкальциемии злокачественных опухолей наиболее эффективны хирургическое удаление основного опухолевого узла, если оно возможно анатомически, индукция клинической ремиссии с помощью химиотерапии (наиболее применимый метод при гиперкальциемии, вызванной LSA) и лучевая терапия.
Эмпирически рекомендуется начало агрессивной терапии при концентрации кальция в сыворотке крови на уровне 16 мг/дл (4 ммоль/л) или выше; однако интенсивность терапии при ведении пациента подбирают индивидуально на основе текущих данных наблюдения и диагностических исследований. Прогноз неблагоприятный у явно ослабленных пациентов при выявлении любого из следующих пунктов:
1. клинические признаки заболевания с гиперкальциемией выше 16 мг/дл (4 ммоль/л);
2. тяжелая почечная азотемия;
3. уровень кальция и фосфора выше 60, что приводит к метастатической минерализации;
4. гиперкальциемия солидных злокачественных опухолей, непригодных для хирургического удаления.
Лечение начинают с агрессивной инфузионной терапии изотоническим (0,9%) раствором хлорида натрия для коррекции дегидратации, часто осложняющей вызываемую гиперкальциемией первичную полиурию (так называемый вторичный нефрогенный несахарный диабет).
Задержку кальция увеличивает сгущение крови, обусловленное снижением клубочковой фильтрации, поскольку почки пытаются сохранить натрий и снижают выведение кальция с мочой (9). Внутривенное введение физиологического раствора в разумных объемах не только восстанавливает гидратацию, но и обеспечивает дополнительное преимущество увеличения объема циркулирующей крови, увеличивающее скорость клубочковой фильтрации и, как следствие, усиливающее кальциурез.
Физиологический раствор не содержит кальция, а содержащееся в нем большое количество натрия конкурирует с кальцием за всасывание в почечных канальцах, что дополнительно способствует выведению кальция (22). После достижения адекватной регидратации показано применение петлевых диуретиков (например, фуросемида по 2–4 мг/кг 2–3 раза в день внутривенно/подкожно/внутрь) в сочетании с продолжением терапии физиологическим раствором, чтобы далее стимулировать выведение кальция с мочой и уменьшить риск развития ятрогенной гиперволемии.
Однако у этих пациентов необходимо соблюдать осторожность, чтобы не допустить обезвоживания, поскольку сгущение крови может свести на нет желаемый кальциурез.
Глюкокортикоиды могут при лечении гиперкальциемии обеспечить быстрый эффект. Однако в идеале вначале следует выявить первопричину заболевания, поскольку неизбирательное назначение глюкокортикоидов потенциально может затруднить установление окончательного диагноза (например, при скрытой опухоли кроветворной системы) или даже оказаться клинически противопоказано (например, при гранулематозных инфекционных заболеваниях).
Глюкокортикоиды способствуют снижению уровня кальция в сыворотке крови путем уменьшения резорбции кальция из костей и всасывания в кишечнике, а также активации выведения кальция почками (22). Они особенно эффективны при лечении гиперкальциемии в рамках злокачественных новообразований, таких как лимфома, AGASACA, миелома, тимома; гипоадренокортицизма, гипервитаминоза D.
Чаще всего назначают преднизолон (1–2,2 мг/кг 2 раза в день внутривенно/подкожно/внутрь) и/или дексаметазон (0,1–0,22 мг/кг 2 раза в день); оба препарата недорогие и широко доступны. Затем дозы соответствующим образом снижают, причем терапию такими высокими дозами нельзя проводить длительно.
Бисфосфонаты — еще один вариант лечения гиперкальциемии; эти препараты разработаны для ингибирования патологической резорбции костей при остеопорозе и метастазах опухолей в кости скелета у человека. В медицине человека чаще всего используют золедронат и памидронат, которые могут нормализовать уровень кальция за 4–10 дней, при этом эффект сохраняется около 1–4 недель (23). Хотя в настоящее время лучше изучено применение памидроната, показана эффективность золедроната при острой гиперкальциемии у собак (24).
Дозы отдельных бисфосфонатов различны, поскольку различаются активность их антирезорбтивного действия и потенциальные побочные эффекты (Рисунок 12). Рекомендуемая доза золедроната составляет 0,1–0,25 мг/кг, разведенного в физиологическом растворе; препарат вводят внутривенно с постоянной скоростью в течение 15–20 минут, а доза памидроната составляет 1,0–2,0 мг/кг, разведенного в физиологическом растворе, и его вводят в течение 2–4 часов.
При назначении этих препаратов важно учитывать, что болюсная инфузия больших доз в доклинических исследованиях токсичности потенциально могла вызвать острое повреждение почек. Хотя вышеуказанные рекомендуемые методы дозирования у ветеринарных пациентов предполагают более длительную продолжительность инфузии и, следовательно, значительно снижают риск повреждения почек, все же рекомендуется во время курса терапии тщательно контролировать функцию почек.
Стоит отметить, что у кошек при персистирующей идиопатической гиперкальциемии исследовалось применение алендроната, принимаемого внутрь бисфосфоната, и была показана его хорошая переносимость (14, 25), но для оценки эффективности, учитывая крайне низкую биодоступность при приеме внутрь, необходимы дальнейшие исследования, и пока неизвестно, следует ли у кошек с персистирующей идиопатической гиперкальциемией рекомендовать его применение прежде других бисфосфонатов.
.png)
Митрамицин, кальцитонин и нитрат галлия теоретически также можно применять для лечения гиперкальциемии, но из‑за высокой стоимости, побочных эффектов и сложного графика введения их клиническая ценность ограничена. Митрамицин (пликамицин) — противоопухолевый антибиотик, ингибирующий синтез РНК в остеокластах, что приводит к быстрому снижению резорбции кости (22).
Этот препарат и в ветеринарии, и в медицине человека стали использовать реже из‑за риска индуцирования тромбоцитопении, некроза почек и печени, а также гипокальциемии. Еще одним вариантом лечения считают кальцитонин, который ослабляет резорбцию костной ткани путем подавления активности и образования остеокластов.
Это приводит к быстрому снижению концентрации кальция в сыворотке крови в течение нескольких часов после введения препарата — быстрее, чем при любых других методах лечения, но из‑за компенсаторной регуляции синтеза рецепторов эффект препарата оказывается относительно кратковременным. Нитрат галлия — противоопухолевый
Заключение
Концентрация ионизированного кальция в организме регулируется очень строго, и ее изменения могут привести к значительным и пагубным системным последствиям для многих органов. Паранеопластическая гиперкальциемия — серьезное и относительно частое осложнение различных опухолей у собак, которое развивается по ряду механизмов изменения гомеостаза кальция, что вызывает клинические проявления.
Из опухолей гиперкальциемию у собак чаще всего вызывает Т-клеточная лимфома, но при выявлении повышенной концентрации кальция следует всегда исключать другие опухоли и неопухолевые заболевания. Хотя клинические проявления гиперкальциемии часто неспецифичны, важно как можно раньше выявить ее причину. После этого назначают этиотропное лечение и поддерживающую терапию, что минимизирует риск развития опасных для жизни осложнений и повышает вероятность благоприятного исхода.
Литература
-
1.Clapham DE. Calcium signaling. Cell. 2007;131(6):1047-1058.
-
2.Hajdu S, Leonard EJ. A calcium transport system for mammalian cells. Life Sci. 1975;17(10);1527-1533.
-
3.Matikainen N, Pekkarinen T, Ryhänen EM, et al. Physiology of calcium homeostasis: an overview. Endocrinol. Metab. Clin. North Am. 2021;50(4):575-590.
-
4.Potts JT. Parathyroid hormone: past and present. J. Endocrinol. 2005;187(3):311-325.
-
5.Silva BC, Bilezikian JP. Parathyroid hormone: anabolic and catabolic actions on the skeleton. Curr. Opin. Pharmacol. 2015;22:41-50.
-
6.Huang JC, Sakata T, Pfleger LL, et al. PTH differentially regulates expression of RANKL and OPG. J. Bone Miner. Res. 2004;19(2):235-244.
-
7.Christakos S, Li S, de la Cruz J, et al. Vitamin D and the intestine: review and update. J. Steroid. Biochem. Mol. Biol. 2020;196:105501.
-
8.Xie J, Guo J, Kanwal Z, et al. Calcitonin and bone physiology: in vitro, in vivo, and clinical investigations. Int. J. Endocrinol. 2020;2020:3236828.
-
9.Daniels E, Sakakeeny C. Hypercalcemia: pathophysiology, clinical signs, and emergent treatment. J. Am. Anim. Hosp. Assoc. 2015;51(5):291-299.
-
10.Coady M, Fletcher DJ, Goggs R. Severity of ionized hypercalcemia and hypocalcemia is associated with etiology in dogs and cats. Front. Vet. Sci. 2019;6;276.
-
11.Elliott J, Dobson JM, Dunn JK, et al. Hypercalcemia in the dog – a study of 40 cases. J. Small Anim. Pract. 1991;32(11):564-571.
-
12.Messinger JS, Windham WR, Ward CR. Ionized hypercalcemia in dogs: a retrospective study of 109 cases (1998-2003). J. Vet. Intern. Med. 2009;23(3):514-519.
-
13.Savary KCM, Price GS, Vaden SL. Hypercalcemia in cats: a retrospective study of 71 cases (1991-1997). J. Vet. Intern. Med. 2000;14(2):184-189.
-
14.Hardy BT, de Brito Galvao JF, Green TA, et al. Treatment of ionized hypercalcemia in 12 cats (2006-2008) using PO-administered alendronate. J. Vet. Intern. Med. 2015;29(1):200-206.
-
15.Goldner W. Cancer-related hypercalcemia. J. Oncol. Pract. 2016;12(5):426-432.
-
16.Mirrakhimov AE. Hypercalcemia of malignancy: an update on pathogenesis and management. N. Am. J. Med. Sci. 2015;7(11):483-493.
-
17.de Papp AE, Stewart AF. Parathyroid hormone-related protein a peptide of diverse physiologic functions. Trends Endocrinol. Metab. 1993;4(6):181-187.
-
18.Weller RE, Hoffman WE. Renal function in dogs with lymphosarcoma and associated hypercalcemia. J. Small Anim. Pract. 1992;33(2):61-66.
-
19.Galvao JFD, Parker V, Schenck PA, et al. Update on feline ionized hypercalcemia. Vet. Clin. North Am. Small Anim. Pract. 2017;47(2);273-292.
-
20.Lebastard M, Cuq B, Sharman MJ, et al. Diagnostic performance of predicted ionized calcium in dogs with total hypercalcemia and total hypocalcemia. Vet. Clin. Pathol. 2021;50(4):515-524.
-
21.Groth EM, Chew DJ, Lulich JP, et al. Determination of a serum total calcium concentration threshold for accurate prediction of ionized hypercalcemia in dogs with and without hyperphosphatemia. J. Vet. Intern. Med. 2020;34(1):74-82.
-
22.Schaer M. Therapeutic approach to electrolyte emergencies. Vet. Clin. North Am. Small Anim. Pract. 2008;38(3):513-533.
-
23.Schenk A, Lux C, Lane J, et al. Evaluation of zoledronate as treatment for hypercalcemia in four dogs. J. Am. Anim. Hosp. Assoc. 2018;54(6);e54604
-
24.Repasy AB, Selmic LE, Kisseberth WC. Canine apocrine gland anal sac adenocarcinoma: a review. Top. Companion Anim. Med. 2022;50;100682
-
25.Kurtz M, Desquilbet L, Maire J, et al. Alendronate treatment in cats with persistent ionized hypercalcemia: a retrospective cohort study of 20 cases. J. Vet. Intern. Med. 2022;36(6):1921-1930.
«Патологическая гиперкальциемия у собак »!
 Заработанные
Заработанные баллы


были начислены ранее
 230
230 дополнительный
материал для скачивания
 574
574  1798
1798 дополнительный
материал для скачивания
 48
48  34
34  66
66 


 116
116  10 мин
10 мин




