Введение
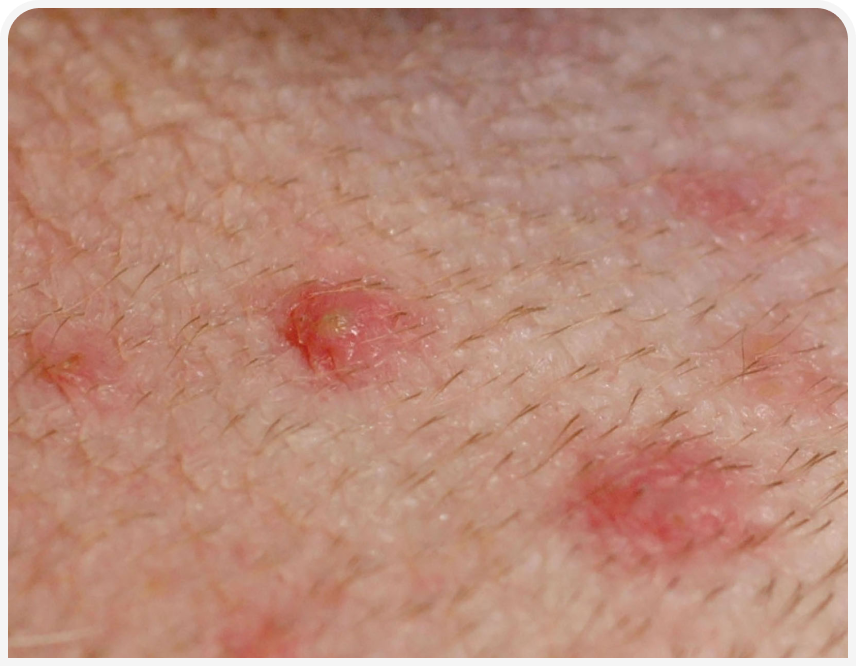
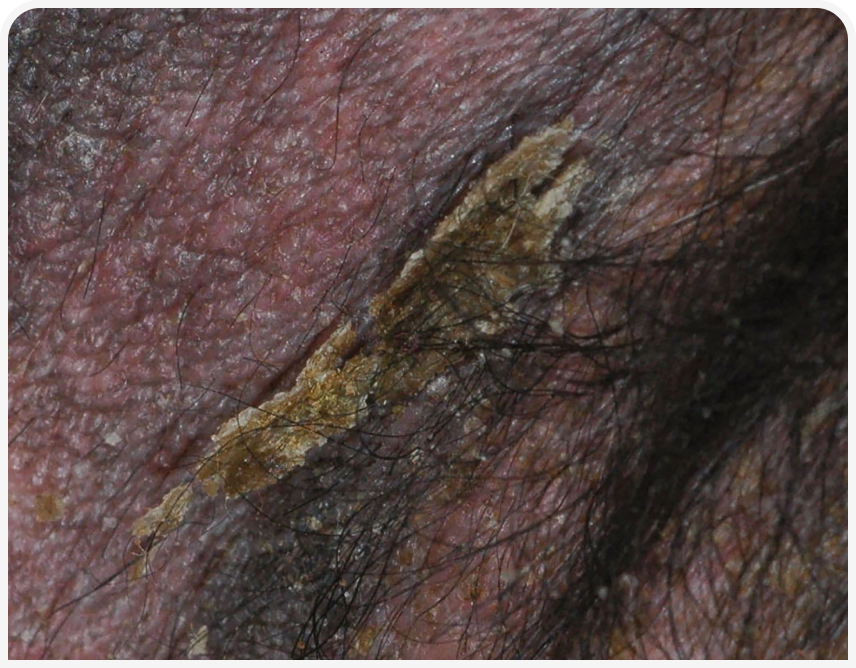
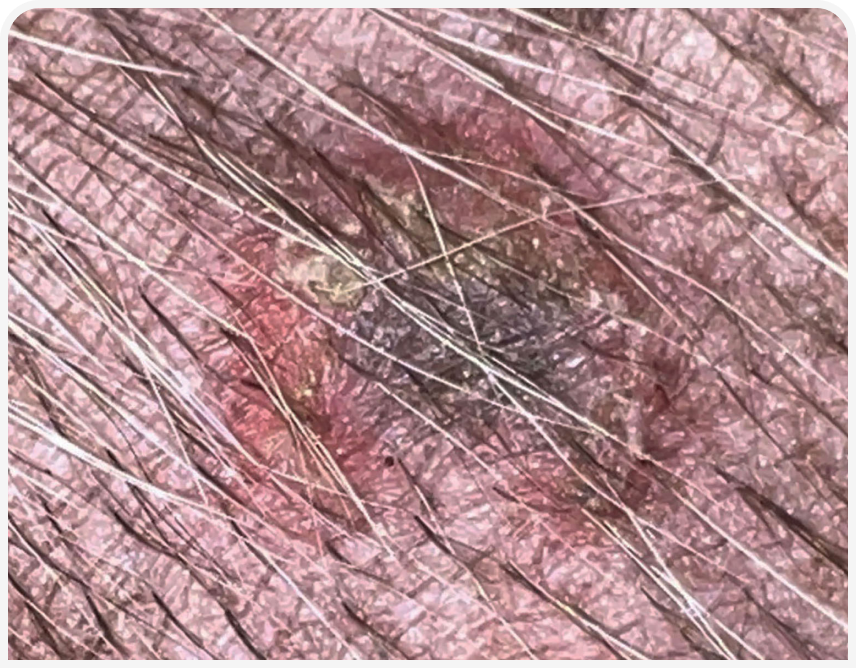
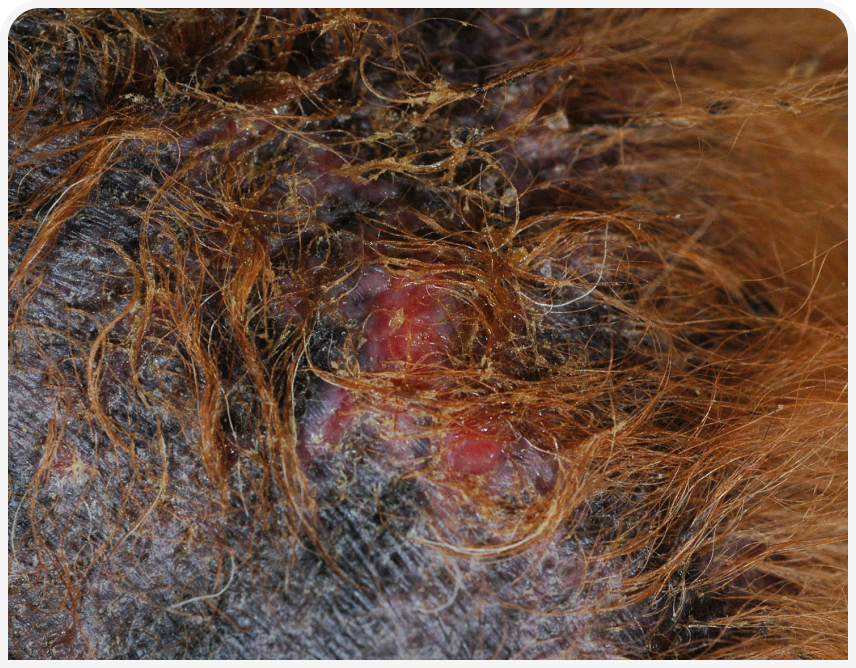
Пиодермия — бактериальная инфекция кожи, которую обычно подразделяют на поверхностную и глубокую в зависимости от пораженного слоя кожи. Клинически поверхностная пиодермия проявляется эритематозными папулами и пустулами (Рисунок 1), которые могут располагаться в центре волосяных фолликулов. На коже также часто появляются корочки медово-коричневого цвета (Рисунок 2), которые могут прилипать к стержням волос. Появляются также эпидермальные воротнички (Рисунок 3) в виде кольцеобразной области шелушения. При более хроническом течении развиваются алопеция, гиперпигментация и язвы (Рисунок 4). Глубокие поражения при пиодермии клинически проявляются язвами и свищевыми ходами (Рисунок 5) (1).
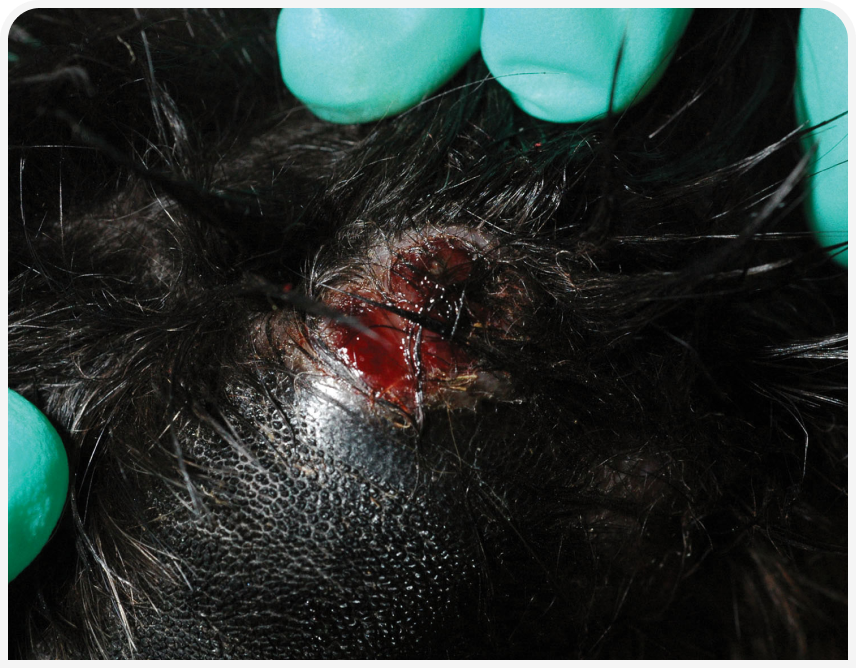
Возбудители
Вызывающие пиодермию бактерии в основном относятся к чрезмерно разросшейся нормальной микрофлоре; чаще всего при пиодермии выявляют коагулазоположительные виды стафилококков. Из них у собак наиболее распространен S. pseudintermedius, а у кошек — S. aureus, другой коагулазоположительный микроорганизм. S. schleiferi — вторая по распространенности бактерия, вызывающая пиодермию у собак, причем этот микроорганизм отличается способностью изменять синтез коагулазы; в некоторых случаях он по коагулазе положительный, а в других — отрицательный (2). Ранее коагулазоотрицательные Staphylococcus spp. считали непатогенными микроорганизмами, но в новых исследованиях было показано, что этот род бактерий (включающий S. epidermidis, S. xylosus и S. Haemolyticus (1, 3, 4)) может быть патогенным. Иногда в качестве этиологического фактора пиодермии выявляют бактерии Streptococcus canis, Pseudomonas aeruginosa, Corynebacterium auriscanis, Escherichia coli и Proteus spp. (1).
Устойчивость к противомикробным препаратам
Бактерии постоянно эволюционируют и приобретают механизмы устойчивости или генетические мутации, а у Staphylococcus spp. хорошо известен ряд генетических мутаций, позволяющих обходить эффект противомикробных препаратов. У S. pseudintermedius в 80–94% случаев развивается мутация гена blaZ, вызывающая устойчивость к бета-лактамам; следовательно, амоксициллин, ампициллин и пенициллин против этого возбудителя неэффективны. Амоксициллин может по-прежнему оставаться эффективным, если его действие усилить, например, сочетанием с клавулановой кислотой (5, 6).
Более серьезные опасения в ветеринарной медицине с точки зрения концепции One Health (концепция Единого здоровья — человека, животных и среды) вызывает мутация гена mecA. Мутантный ген кодирует измененный пенициллинсвязывающий белок (PBP2a), имеющий низкое сродство ко всем β-лактамам, включая пенициллины, цефалоспорины и карбапенемы, что означает, что β-лактамы не могут связываться со стенкой бактериальной клетки и убивать микроорганизм. Эта генетическая мутация называется метициллин-резистентным стафилококком (methicillin-resistant staphylococcus — MRS) с последующим указанием вида микроорганизма; например, метициллин-резистентный стафилококк Staphylococcus pseudintermedius (MRSP) и метициллин-резистентный золотистый стафилококк Staphylococcus aureus (MRSA) (2, 7). Разработано новое поколение цефалоспоринов, эффективных против MRSA, но их следует резервировать для применения в медицине человека. Для MRS характерно проявление устойчивости к комбинации других лекарственных средств, включая аминогликозиды, хлорамфеникол, фторхинолоны, линкозамид, тетрациклины, потенцированные сульфаниламиды, рифампицин. Эти случаи можно рассматривать как примеры множественной лекарственной устойчивости (МЛУ), если они устойчивы к двум дополнительным классам противомикробных препаратов, или широкой лекарственной устойчивости (ШЛУ), если они устойчивы ко всем классам противомикробных препаратов, кроме двух или менее (2, 7).
MRSP был впервые обнаружен у животных в 2005 году в Бельгии (8) и с тех пор был выявлен у животных в большинстве стран, если не во всех странах. Однако его распространенность географически весьма вариабельна, что может быть связано с различиями в руководствах по лечению противомикробными препаратами и ограничениями на их применение. В 2011 году распространенность MRSP составляла 0–4,5% у собак в целом и до 7% у собак с кожными заболеваниями. В то время к метициллину, в зависимости от страны, были устойчивы от 30 до 66% изолятов S. pseudintermedius (9). В проведенном недавно в США исследовании было показано, что распространенность изолятов S. pseudintermedius, устойчивых к оксациллину (определяющий фактор устойчивости к метициллину), статистически значимо возросла в период с 2010 по 2021 год (10), а в другом исследовании в США было показано увеличение распространенности MRSP с 28% в 2010 году до 80% в 2020 году (11). За последние 10 лет его распространенность во всем мире значительно возросла.
Из факторов риска в одном исследовании было отмечено, что у собак, получавших лечение противомикробными препаратами в течение последнего месяца, повышался риск развития MRSP по сравнению с чувствительным к метициллину Staphylococcus pseudintermedius (MSSP) (5). В другом исследовании было показано, что у животных, получавших антибиотики, в течение последующего года будет повышен риск развития множественной лекарственной устойчивости (11). Развитие MRSP также оказалось связано с предшествующим воздействием фторхинолонов (12).
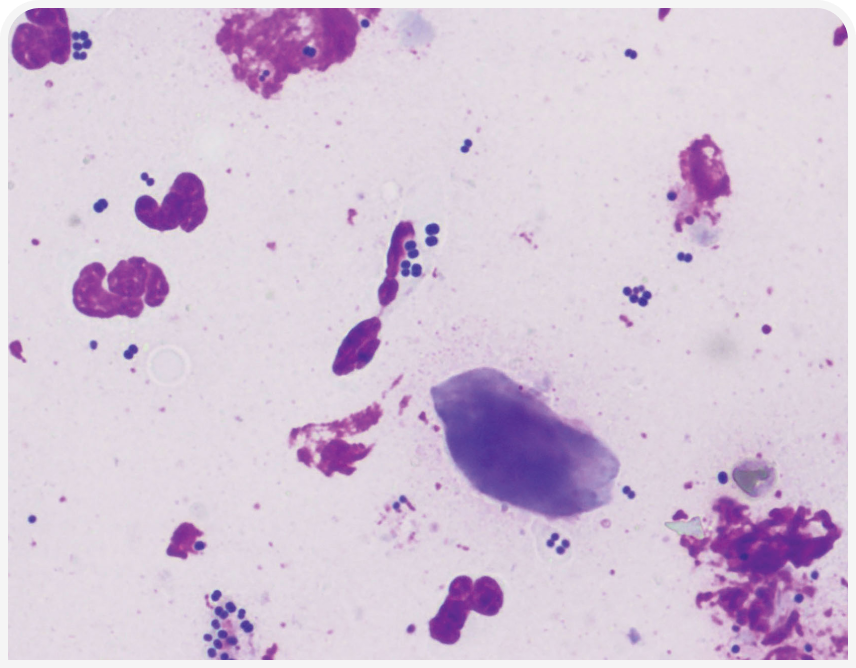
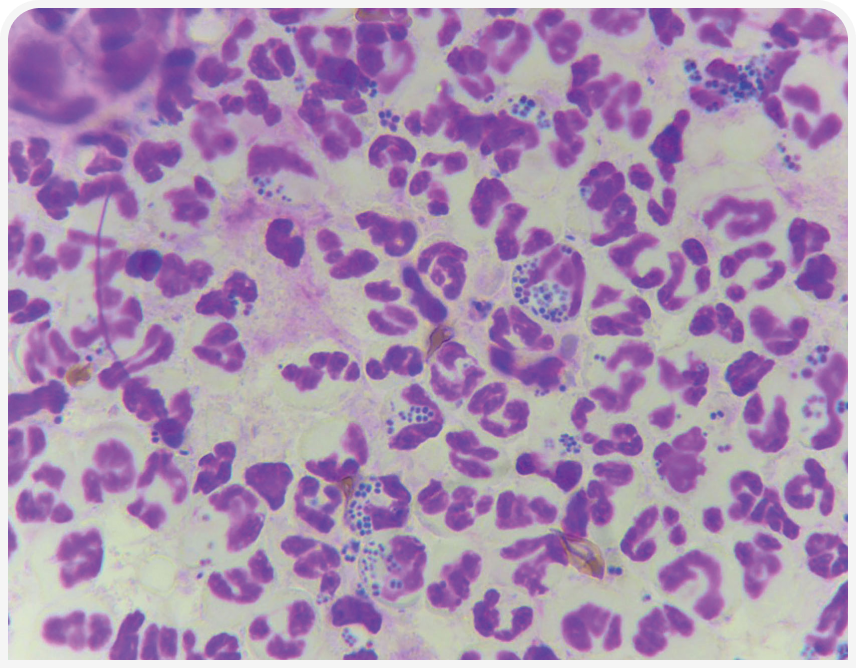
Для диагностики пиодермии проще и эффективнее всего провести цитологическое исследование клинических поражений (пустул, корочек, эпидермальных воротничков). Существует множество способов сделать это, включая мазок-отпечаток, цитологическое исследование пробы клейкой лентой, ватным тампоном и метод суспензии (13). Метод получения образцов выбирают в зависимости от свойств изучаемого поражения. Например, из пустулы и язвы легко получить прямой мазок-отпечаток, поскольку в них присутствует экссудат. Наилучшим способом для изучения корочек и эпидермальных воротничков вследствие их сухости может быть цитологическое исследование пробы клейкой лентой. Наличие воспалительных клеток с ассоциированными бактериями (Рисунок 6) свидетельствует в пользу пиодермии, и диагноз подтверждается, когда внутри воспалительных клеток выявляют кокки (Рисунок 7) (1).
Если эмпирическая противомикробная терапия оказалась неэффективна, системный противомикробный препарат подбирают по результатам бактериального посева с оценкой чувствительности. Проводить посев при пиодермии полезно в любом случае, но при ряде критериев посев настоятельно рекомендуется. Современные рекомендации по проведению бактериального посева с оценкой чувствительности следующие:
1. двух недель соответствующей системной антимикробной терапии;
Из пустул получать образцы удобнее всего, поскольку пустулы можно вскрыть и получить образец культуральным тампоном. Если присутствует гнойный экссудат, культуральным тампоном также удобно получить образец из‑под корок. Если очаг поражения полностью сухой, например в форме корочки или эпидермального воротничка, тампон для культивирования, перед тем как брать соскоб с кожи, лучше пропитать физиологическим раствором. Показано, что это позволяет получить большее по сравнению с сухим тампоном количество бактерий (14). При получении образцов любым из вышеперечисленных методов проводить какую-либо дезинфекцию поверхности кожи не требуется. Однако если для посева тканей планируется проведение биопсии кожи, поверхность рекомендуется обработать, удалив загрязнения (1).
Лечение поверхностной пиодермии можно проводить местно, системно либо комбинированно. С увеличением устойчивости к противомикробным препаратам наблюдается тенденция к использованию большего количества местных средств вместо системных противомикробных препаратов (10). В одном исследовании сравнивалось лечение поверхностной пиодермии собак системными противомикробными препаратами (амоксициллин-клавулановая кислота) или местным шампунем и раствором хлоргексидина в течение четырех недель, и различий выявлено не было (15).
Местную терапию ранее недостаточно использовали для лечения поверхностной пиодермии (1), но по сравнению с системным лечением у нее есть преимущество — возможность достичь более высокой концентрации лекарственного средства. Кроме того, поскольку препараты наносят непосредственно на кожу, препарат не метаболизируется и его концентрация не снижается. Начиная местную терапию, необходимо принять два решения: 1) выбрать активный ингредиент и 2) выбрать наилучшую для данной ситуации лекарственную форму.
Из активных ингредиентов наиболее доступен и часто используется хлоргексидин. Его выпускают в нескольких концентрациях (2–4%) и в составе некоторых препаратов сочетают с противогрибковыми средствами, такими как миконазол, кетоконазол или климбазол. В некоторых исследованиях было продемонстрировано, что концентрация хлоргексидина напрямую не коррелирует с эффективностью; например, эффективность шампуня с 4%-ным хлоргексидином не выше, чем у шампуня с 2%-ным хлоргексидином + 2%-ным миконазолом. Эффективность хлоргексидина при лечении как MRSP, так и MSSP одинаковая, и, хотя часто встречается устойчивость к хлоргексидину, доказательств ее клинической значимости нет (16).
Несколько реже хлоргексидина из активных ингредиентов используют бензоилпероксид и этиллактат. Показано, что бензоилпероксид эффективен при лечении поверхностной пиодермии, но его выпускают в очень ограниченном числе лекарственных форм. Данные о его эффективности различаются, но следует отметить, что для оценки истинной активности бензоилпероксида необходимы исследования in vivo, поскольку при взаимодействии с кожей образуются высокореактивные кислородные радикалы, весьма эффективные против бактерий. Этиллактат во многих аспектах аналогичен бензоилпероксиду, но количество его лекарственных форм также ограничено, и для оценки его истинной активности также необходимы исследования in vivo, чтобы оценить взаимодействие с кожей после его гидролизации до этанола и молочной кислоты (16).
Из новых активных ингредиентов при лечении поверхностной пиодермии показали эффективность гипохлорит натрия, форсированная перекись водорода (accelerated hydrogen peroxide — AHP), соединения серебра, эфирные масла, растительные экстракты. Ранее было показано, что разбавленный отбеливатель, активным компонентом которого является гипохлорит натрия, эффективен против S. pseudintermedius (16), причем его кожная переносимость у здоровых собак сохраняется при разбавлении до 0,005% (17). В некоторых странах гипохлорит натрия в сочетании с салициловой кислотой выпускают в форме шампуня. Также показана эффективность форсированной перекиси водорода в форме шампуня. В качестве активного ингредиента при использовании в сочетании с другими, такими как хлоргексидин, перспективны соединения серебра, причем в нескольких лекарственных формах. В состав средств для местного лечения или профилактики пиодермии добавляют ряд эфирных масел и растительных экстрактов (16).
Для местного применения предложено множество лекарственных форм, включая шампуни, спреи, салфетки, муссы, ополаскиватели, кондиционеры, гели, кремы, мази. Чтобы выбрать предпочтительную лекарственную форму, следует оценить распространенность поражения: генерализованное, локализованное или очаговое. При генерализованных поражениях лучше применять шампуни, спреи, муссы, ополаскиватели и кондиционеры. При локализованных или очаговых поражениях целесообразно использовать салфетки, гели, кремы и мази. Шире всего из лекарственных форм на сегодняшний день применяют шампуни с широким спектром активных ингредиентов. Обычная схема применения шампуней, спреев и муссов: 2–3 раза в неделю до разрешения поражений и еще 7 дней после этого, при этом время контакта шампуней с кожей до ополаскивания должно составлять 10 минут. Салфетки, гели, кремы и мази следует использовать ежедневно (1).
Наконец, недавно для лечения глубокой и поверхностной пиодермии было предложено применять флуоресцентную световую энергию. По этой методике флуоресцентное освещение выбивает из геля с хромофорами фотоны с различными длинами волн, проникающие глубоко в кожу и оказывающие там биологическое действие, способствующее восстановлению кожи и повышающее в ней антимикробную активность. Показано, что при лечении поверхностной пиодермии эта методика в качестве монотерапии лучше, чем системные противомикробные препараты, купирует клинические поражения и ускоряет излечение (18).
Системную антимикробную терапию поверхностной пиодермии в настоящее время рекомендуют проводить в течение 21 дня, или одну неделю после разрешения клинических проявлений, а глубокие пиодермии рекомендуется лечить в течение 6 недель, или 2 недели после разрешения клинических проявлений. Изучение этих рекомендаций продолжается, и в будущем они могут измениться. Для лечения глубокой пиодермии требуется системная терапия, поскольку местным терапевтическим средствам трудно достичь инфицированной области. Так как основой лечения считают противомикробные препараты, для терапии поверхностной пиодермии разработаны рекомендации по выбору противомикробных препаратов первого, второго и третьего ряда (Таблица 1). Противомикробные препараты первого ряда применяют эмпирически, без проведения посева. Цефалоспорины третьего поколения помещены в серую зону первого/второго ряда, поскольку могут усиливать отбор грамотрицательных микроорганизмов, устойчивых к противомикробным препаратам, в других участках тела. Противомикробные препараты второго ряда следует использовать только после посева и подбирать с учетом чувствительности возбудителя. Противомикробные препараты третьего ряда следует использовать, если другого варианта лечения инфекции нет, так как они предназначены для применения в медицине человека. Поскольку поверхностные пиодермии можно лечить местно, противомикробные препараты третьего ряда в этой ситуации не показаны; единственным показанием для их применения считают глубокую пиодермию, требующую системной терапии (1).
В одном исследовании была изучена динамика изменения устойчивости к противомикробным препаратам в период с 2010 по 2021 год в США. Было обнаружено значительное повышение устойчивости к клиндамицину, амоксициллину-клавулановой кислоте, оксациллину, цефокситину, цефподоксиму, тетрациклину, хлорамфениколу, эритромицину, марбофлоксацину и гентамицину. Повышения устойчивости за этот период не было выявлено только для цефалотина и сульфаниламидов (10). Это свидетельствует о необходимости следовать рекомендациям по противомикробной терапии и разумно использовать системные противомикробные препараты первого, второго или третьего ряда.
Важно отметить, что после разрешения пиодермии нормальной флорой с высокой вероятностью окажется тот же микроорганизм, против которого было направлено лечение; в одном исследовании почти у половины (45,2–47,6%) собак с вызванной MRSP пиодермией после разрешения инфекции MRSP был обнаружен либо на коже, либо в области носительства (19). Почти такую же тревожность вызывает тот факт, что после успешного излечения вызванной MSSP пиодермии у 38,3% собак впоследствии на коже или в области носительства был обнаружен MSSP (19). Попытки деколонизировать инфекцию MRSP у собак, аналогично мероприятиям при инфекции MRSA у человека, оказались неэффективны. Кроме того, было показано, что у бессимптомных контактных собак положительный результат тестирования фиксировался с той же частотой, что и у инфицированных MRSP собак (67,4% против 66,7%), что демонстрирует риск передачи бактерий при контакте с собаками в доме (20). Статус носительства MRSP в этом исследовании затем периодически отмечался в течение 10 месяцев, что служит основанием для рекомендации проведения посева у инфицированного пиодермией животного, если в течение последнего года у него выявлялся MRSP.
Пиодермия в большинстве случаев развивается на фоне другого заболевания, и для профилактики рецидива необходимо выявить это первичное заболевание, оценить его тяжесть и вылечить (1). У собак пиодермии часто предшествует атопический дерматит, и в таких случаях целью лечения считают купирование атопии, чтобы предотвратить чрезмерное применение противомикробных препаратов. В Австралии было проведено исследование собак с атопическим дерматитом, которые получали лечение оклацитинибом; по сравнению с контрольной группой курсов терапии противомикробными препаратами этим собакам требовалось меньше (21). Для профилактики пиодермии и уменьшения частоты рецидивов и тяжести клинических проявлений атопического дерматита может быть полезна диета; в одном исследовании было показано значимое уменьшение выраженности атопического дерматита у собак, получавших соответствующую диету на протяжении 9 месяцев (22).
При лечении пиодермии владельцы часто беспокоятся, не заразятся ли они сами. Некоторый риск передачи бактерий от домашнего животного к владельцу и наоборот существует (1). В проведенном на Тайване исследовании было продемонстрировано, что риск инфицирования S. pseudintermedius повышается у владельцев трех или большего количества собак, а также у владельцев, которые позволяют собаке лизать свое лицо (5). Если владельцы оказались колонизированы MRSP от животного, генетическая мутация MRSP может затем переноситься в нормальную микрофлору Staphylococcus spp. у владельца, что может создавать для него риск инфицирования MRS (7).
Устойчивость микроорганизмов при пиодермии значительно повышается. Поэтому местную терапию следует считать методом первой линии лечения, что позволяет предотвратить дальнейшее мутационное давление на бактерии, формирующее у них устойчивость к системным противомикробным препаратам. Если требуется применить системные противомикробные препараты, крайне важно соблюдать последовательность их применения; противомикробные препараты 1-го ряда идеально подходят для эмпирической терапии, но противомикробные препараты 2-го ряда следует использовать, только если чувствительность к ним подтверждена результатами посева. Распространенность и факторы риска
Диагностика
Цитология
Бактериальный посев
2. появление новых клинических поражений (папул, пустул, эпидермальных воротничков, корочек) через две или более недель после проведения соответствующей антимикробной терапии при цитологически диагностированной пиодермии;
3. сохранение клинически выявляемых поражений после шести недель антимикробной терапии, диагноз «пиодермия» подтвержден при цитологическом исследовании;
4. при цитологическом исследовании выявлены внутриклеточно расположенные палочковидные бактерии;
5. инфекции с множественной лекарственной устойчивостью в анамнезе животного, в том числе домашнего (1).
Эксперт-квиз по диагностике зудаЛечение
Местная терапия

Системная терапия
 КАРТИНКА
КАРТИНКА
Статус носительства
Профилактика рецидивирующей пиодермии
Риск развития зооноза
Заключение


телефона ниже для сброса пароля.


на номер
+7 {{ formatted_phone }}

Вы успешно прошли тест!
{{ countries[country][1] }}
{{ value[0] }}
{{ formatted_phone }}.
Введите последние четыре цифры номера входящего звонка.

весь модуль
всех видеоуроков модуля














 4313
4313  10 мин
10 мин



.png)




