Введение
Согласно научным литературным источникам, иммунология — это общебиологическая наука, изучающая защитные реакции организма, направленные на сохранение его структурной и функциональной целостности и биологической индивидуальности (1). Иммунология как наука за весь период своего становления и существования решала важнейшие вопросы, прежде всего, механизмов иммунного ответа и методов борьбы с распространением особо опасных инфекционных заболеваний как в гуманной, так и в ветеринарной медицине.
Именно по причине таких приоритетных для мировой науки и общества задач данная отрасль медицины стала крайне активно развиваться и характеризовалась множественными «прорывными» открытиями с самого своего формирования (1;2). Однако, разве мы можем сказать, что в современной медицинской и ветеринарной науке иммунология стала доступным инструментом в лабораторной диагностике широкого спектра заболеваний и состояний в рутинной практике для каждого ветеринарного врача?
Что мы — ветеринарные врачи, понимаем физиологию и патогенез иммунологических механизмов, обусловливающий развитие патологических состояний у наших пациентов? Что мы понимаем аспекты выявления индивидуальных иммунных особенностей у наших пациентов при конкретных состояниях
и причины неэффективности стандартной терапии для ряда пациентов?
Так как на данный момент, несмотря на интенсивное развитие фундаментальной и прикладной ветеринарной медицины, ветеринарная иммунология и, в частности, многие компоненты аутоиммунного ответа / воспаления, достаточно изученные в гуманной медицине, остаются малодоступными для исследования и, как следствие — для практического применения в лабораторной диагностике ветеринарными врачами.
Это, как нам кажется, большая проблема современной ветеринарной медицины, так как мы — врачи, используя выработанные навыки клинического мышления, опираемся на унифицированные механизмы протекания физиологических и патофизиологических процессов, не имея базы и ресурсов для комплексного понимания индивидуального аутоиммунного статуса пациента.
Вспомним, основные компоненты иммунной системы в классическом ее представлении (рисунок 1).
В свою очередь, гуманная медицина уже доказала необходимость исследования множества компонентов иммунного и аутоиммунного генеза для определения рисков, осложнений и прогноза протекания многих заболеваний, а также для улучшения качества жизни пациентов с использованием ресурсов предиктивной персонализированной медицины.
На базе сети ветеринарных клиник «Василек» в рамках научно-исследовательской деятельности мы провели статистическое исследование, основанное на данных анкетирования практикующих ветеринарных врачей общей практики и специалистов, являющихся сотрудниками наших клиник.
По результатам его 54,2% респондентов (из 24 человек) полностью или практически полностью не владеют какими-либо данными о специфических факторах коагуляции и вопросах их интерпретации в практике, а также считают актуальным и необходимым изучение и внедрение их лабораторной диагностики в рутинную диагностику для пациентов с нарушениями свертываемости крови в анамнезе.
Наше мнение заключается в том, что крайне актуальным является изучение и внедрение оценки и интерпретации аутоиммунных факторов в практическую деятельность ветеринарных врачей всех направлений. Для этого представляется необходимым выделить иммунологию в отдельную самостоятельную область ветеринарной медицины, тесно связанную с другими узкими направлениями, не на кафедральном уровне, а на практическом.
Ведь как мы можем наблюдать, аутоиммунные компоненты в протекании хирургических, травматологических, гастроэнтерологических, репродуктивных, дерматологических заболеваний, инфекционных заболеваний, а также осложнений в трансфузионной практике и трансплантологии, потенциально способны оказывать значительное влияние (3).
Рассмотрим один из аутоиммунных маркеров, такой как — антинуклеарный фактор или антинуклеарные антитела (АНФ/ANA). Антинуклеарные антитела (ANA) представляют собой спектр аутоантител, которые реагируют со структурами клеточного ядра. Анализ ANA в гуманной медицине — рутинный скрининговый тест для диагностики аутоиммунных заболеваний в практике врачей репродуктологов, ревматологов, иммунологов.
Например, есть исследования, которые подтверждают прямую корреляцию положительных ANA (антинуклеарных антител) у пациентов c первичной иммунной тромбоцитопенией (ИТП) на доклинической стадии заболеваний соединительной ткани (3), взаимосвязь ANA и ревматоидного фактора (RF) c тяжестью течения COVID-19 (4), также может служить общим маркером системного воспаления (5), и косвенным маркером ряда внутриклеточных инфекционных агентов (6).
Тогда как в ветеринарной медицине сложно найти даже теоретический материал относительно ANA и его интерпретации в практике, есть единичные исследования, не доказывающие его информативность в отношении какой-то определенной патологии (7).
Другой немаловажный и широко изученный в медицинской науке аутоиммунный маркер — это ревматоидный фактор (RF). Он представляет собой аутоантитела IgG, IgM, IgA и IgE классов, реагирующие с Fc-фрагментом IgG и образуется в результате стимуляции агрегированным модифицированным IgG или за счет воздействия экзогенного перекрестнореагирующего АГ при нарушении иммунорегуляции.
Комплекс IgG+ревматоидный фактор не фагоцитируется, откладывается в периваскулярном пространстве, стимулируя клеточно-опосредованные цитотоксические реакции, что и обуславливает развитие воспаления. Он является основным при диагностике аутоиммунных поражений суставной ткани и широко используется в гуманной медицине (8-11). Таким образом, относительно ANA ревматоидный фактор и его корреляция с различными патологическими состояниями у животных в ветеринарной науке изучается более интенсивно, хотя и не имеет рутинной практики применения.
Нельзя не уделить внимание таким потенциально клинически значимым в трансфузиологии, терапии и хирургии диагностическим критериям, как целая группа факторов коагуляции. В практике ветеринарных врачей чаще всего мы сталкиваемся с необходимостью оценки фактора Виллебранда, а также факторов 7-го, 8-го и 9-го факторов свертываемости, так как обычно встречаются нарушения коагуляции именно по причинам их недостатка (не беря во внимание фитометадионовую недостаточность вследствие воздействия гемолитических ядов).
Фактор Виллебранда — Фактор фон Виллебранда (ФВ) — мультимерный гликопротеин плазмы крови, который присутствует в эндотелиальных клетках, мегакариоцитах, тромбоцитах и соединительной ткани. Он опосредует адгезию тромбоцитов в условиях артериального кровотока. ФВ также связывает и защищает от деградации фактор свертывания крови VIII.
Было показано, что ФВ участвует в воспалении, опосредуя связь между гемостазом и воспалением (рисунок 2). Мультимеры ФВ и тромбоциты, прикрепленные к поврежденному или активированному эндотелию, опосредуют рекрутирование лейкоцитов, что создает условия для распространения воспалительной реакции.
Нарушение функций ФВ, врожденные дефекты, дефицит синтеза его мультимеров или усиление протеолиза приводят к кровотечениям как при болезни Виллебранда, так и при синдроме Хейда у людей, его патологическая активация может приводить к развитию тромботических осложнений ишемической болезни сердца у людей (12).
Фактор Виллебранда (WF) и его недостаточность уже достаточно изучены у собак и доказана генетическая предрасположенность к его снижению у определенных пород, что является причиной развития болезни Фон Виллебранда.
К ним относятся: австралийский лабрадудль (Коббердог), австралийский терьер, барбет, бассет-хаунд, бернедудель, бернский зенненхунд, бразильский терьер, вельш-корги кардиган, вельш-корги пемброк, вест-хайленд-уайт-терьер, вольфшпиц (Кеесхонд), голдендудль, доберман, дрентская куропаточная собака (Дрентский партийсхонд), золотистый ретривер, ирландский сеттер (красный и красно-белый), кавапу, керри-блю терьер, кокапу, котон-де-тулеар (Мадагаскарский бишон), кромфорлендер, лабрадудль ориджинал, мальтипу, манчестер-терьер, немецкая овчарка, ньюфипу, папийон, немецкий пинчер, пудель (все разновидности), ротвейлер, стабихун, фален, цвергпинчер, цвергшнауцер (13).
Болезнь Фон-Виллебранда (БВ) может быть трех типов, но мы не видим необходимым рассматривать их клинические особенности в контексте данной работы. БВ первого типа является самой распространенной и имеет, в основном, аутосомно-рецессивный характер наследования, в связи с чем крайне редко может встречаться у беспородных собак и редко – у метисов (14).
Однако, у породы Кромфор — ландер наследование, вероятнее всего, происходит по аутосомно-доминантному способу с неполной пенетрантностью, на чем основаны результаты одного из научных исследований (15). Диагностика заболевания проводится с помощью определения WF и фактора 8 в крови, а также на основании генетических тестов. Терапия — заместительная.
Кроме очевидной взаимосвязи концентрации WF в сыворотке крови с коагулопатиями, а также ассоциациями с другими заболеваниями, показанными в исследованиях гуманной медицины, еще имеются научные данные о прямой корреляции уровня WF со степенью прогрессирования печеночной недостаточности у собак, что говорит о потенциальной эффективности использования данного лабораторного показателя как одного из маркеров поражения печени (16).
Также для WF была обнаружена роль в ангиогенезе и в том числе в формировании сосудистых мальформаций, однако молекулярные механизмы, подробно объясняющие этот процесс, пока остаются малоизученными (17). Такие многочисленные функции данного белка открывают нам гораздо более широкие возможности для использования определения сывороточного WF в ветеринарной лабораторной диагностике.
Следующие факторы, играющий важнейшую роль в гемостазе, которые мы не можем не обсудить, это — факторы свертываемости 8 и 9. Данные белки являются важнейшими факторами гемостаза и синтезируются в печени, а также – эндотелии сосудов (FVIII). Врожденная (генетически обусловленная) или приобретенная недостаточность FVIII, FIX вызывает развитие гемофилии типа А или В (соответственно). FVIII, в свою очередь, как мы уже описали выше, тесно связан с WF, так как образует с ним комплексы.
Фактор свертывания крови VIII (FVIII) — это неэнзиматический кофактор активированного фактора IX (FIXa), который при протеолитической активации образует с FIXa плотный нековалентный комплекс, связывающий и активирующий фактор X (FX). Дефекты гена FVIII у людей могут приводить к развитию гемофилии А - Х-связанного рецессивного генетического заболевания с частотой встречаемости около 1 случая на 5000 мужчин (18).
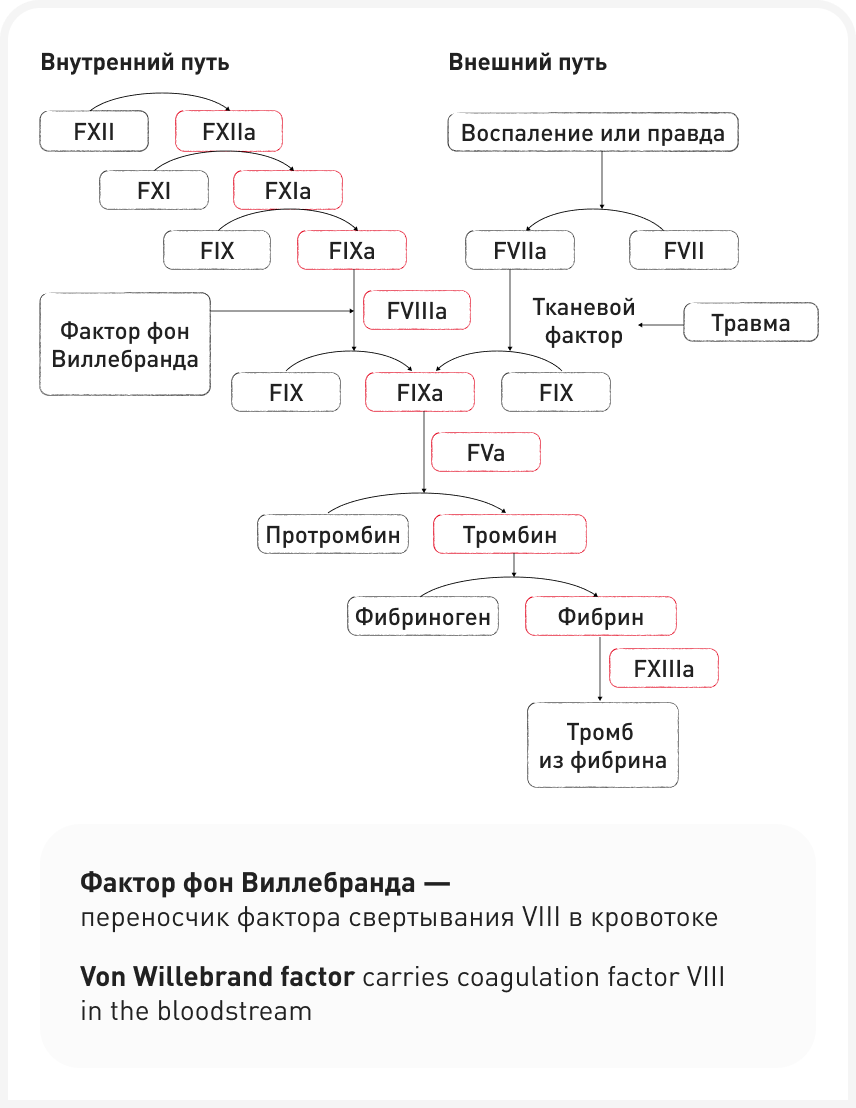
Плотный нековалентный комплекс FVIIIa и FIXa образуется на поверхности фосфолипидной мембраны и дополнительно включает молекулу FX, активируемую FIXa. FX покидает комплекс после активации и запускает, в свою очередь, реакцию превращения протромбина в тромбин (FII в FIIa), который превращает фибриноген в основной компонент тромба — фибрин. Тройной комплекс факторов свертывания FIXа, FVIIIa и FX, связанных с фосфолипидной мембраной, обычно называемый «X-аза», или «теназа», представляет собой основной элемент петли положительной обратной связи в каскаде свертывания крови.
Функционально аналогичный теназе комплекс может быть описан для внешнего пути свертывания (FIII, FVIIa, FIX, FX), однако его энзиматическая эффективность значительно ниже, чем у «внутренней» теназы. Уникальной особенностью теназного комплекса является огромная степень усиления каталитической эффективности малоактивной протеиназы FIXa, сообщаемая FVIIIa – около пяти порядков (рисунок 3).
На настоящий момент в практической гуманной медицине успешно проводят заместительную терапию фактором 8 при гемофилии. Применяют лекарственные препараты рекомбинантного полноразмерного FVIII. Существует 3 поколения препаратов данной группы, которые имеют непринципиальные отличия между собой, поэтому мы не будет останавливаться на них (18).
Тем временем, в ветеринарной медицине, схемы заместительной терапии адаптированными для животных препаратами нет. Также стоит отметить, что в отношении гемофильных состояний у собак и кошек, в основном, описаны только методы диагностики. Фактор свертывания крови IX является гликопротеином, зависимым от витамина К. (19). Он представляет из себя профермент протеазы, играющей центральную роль в каскаде свертывания крови. Для подробной характеристики гемофилии В, вызываемой недостатком фактора свертывания IX, обратимся к гуманной медицине.
Гемофилия В — это рецессивное, Х-сцепленное нарушение свертываемости крови, обусловленное наследственным дефицитом данного витамин К-зависимого фактора свертывания IX (FIX) (20). Уровни активности FIX, четко не коррелирует с фенотипом кровотечения, вероятно, из-за многокомпонентности процесса гемостаза.
Даже медицинские специалисты в области гемостаза говорят о том, что приветствуется расширение знаний о факторах, влияющих на изменения гемостатической функции и клинических исходов, а также реакции на терапию. Особенность FIX в том, что он действует на пересечении как внешних, так и внутренних путей гемостаза, а также на прокоагулянтную мембрану тромбоцитов очагово в ответ на поражение кровеносных сосудов, и, следовательно, биология FIX нацелена на множество эффекторов и регуляторов.
Синтез, клеточные и молекулярные взаимодействия, а также пути выведения FIX изучены не так хорошо, как для FVIII даже в гуманной медицине (20) Особый интерес как для медицинской, так и для ветеринарной гематологии, представляет специфическая роль магния как в процессе адгезии тромбоцитов, так и в активации FIX и сосудистого коллагена в гемостатическом участке адгезии тромбоцитов.
Очевидно, что при любых нарушениях гемостаза и патологических процессах в других тканях соединительного типа, магний и предшественники коллагена (аскорбиновая кислота, лизин, пролин) необходимы как компонент комбинированной терапии для стабилизации тонуса сосудов кровеносного и лимфатического русла.
Однако, если в гуманной медицине узкие специалисты-гемостазиологи применяют препараты магния, а также предшественники коллагена достаточно широко и успешно в составе комбинированной терапии различных типов недифференцированных дисплазий соединительной ткани, в том числе аутоиммунного генеза, то в ветеринарной медицине в принципе не существует ни схемы дозирования, ни рекомендаций по подбору препаратов, тем более — по режиму применения и длительности курсов терапии, что является особо перспективным для проведения исследований в ветеринарии.
Таким образом, мы делаем вывод о том, что «пробелов», вопросов и задач современная гемостазиология в ветеринарии на данном этапе своего становления оставляет значительно больше, чем достоверных данных. Для ветеринарных специалистов «золотым стандартом» диагностики гемофилии типа А и В у собак служит генетический тест, проводимый ветеринарными лабораториями.
Углубляясь в вопросы диагностики, мы хотели бы подчеркнуть, что рутинным и известным методом установления различных патологий гемостаза у собак (болезнь Виллебранда, гемофилия А, гемофилия В) является генетическое исследование на известные, ассоциированные с этими заболеваниями, мутации соответствующих генов.
При этом мы рутинно не проводим и не имеем практической возможности проводить исследование наличия и уровней сывороточных факторов свертываемости. Открыт вопрос в принципе о том насколько они видоспецифичны, а также о критериях оценки их дефицита. Кроме того, при теоретической возможности получить результаты анализов сывороточных уровней данных факторов стоит задача правильной интерпретации результатов при индикации их дефицита относительно (в перспективе выведенных видовых норм).
Например, при снижении уровней одного из факторов в разной степени следует не только сделать вывод о нарушении гемостаза, а также правильно оценить причинно-следственную связь данного факта и наличия кровотечений в анамнезе, так как недостаток факторов свертываемости могут быть как причиной геморрагического синдрома различной степени, так и следствием кровопотери.
Актуальность
.png)
Аутоиммунные маркеры
.png)
Выводы и рекомендации ветеринарным врачам
«Вопросы иммунологии
и патогенеза нарушений гемостаза у животных»!
баллы


были начислены ранее

.png)






телефона ниже для сброса пароля.



на номер
+7 {{ formatted_phone }}


Вы успешно прошли тест!
зарегистрироваться/авторизоваться
способ авторизации/регистрации.
{{ formatted_phone }}.
Введите последние четыре цифры номера входящего звонка.

весь модуль
всех видеоуроков модуля














 87
87  10 мин
10 мин




