Введение
Для лабораторной оценки состояния печени требуется собрать минимальную базу данных, включая общий (ОАК, CBC) и биохимический анализы крови, анализ мочи. Основная часть данных непосредственно для изучения состояния и функции печени содержится в биохимическом профиле, но сам по себе он не позволяет дифференцировать первичные и вторичные заболевания печени.
Их разделяют на основании обобщения всех имеющихся данных, причем в некоторых случаях это оказывается невозможно: например, у собак с иммуноопосредованной гемолитической анемией (immune-mediated hemolytic anemia — IMHA, ИОГА) на функцию печени влияют гипоксия и воспалительные цитокины, поэтому часто наблюдаются биохимические признаки холестаза и повреждения гепатоцеллюлярной системы (1–4). Общий анализ крови необходим для распознавания основного заболевания крови и подтверждения вторичного характера поражения печени.
Сывороточные биомаркеры, используемые в клинических условиях для оценки состояния печени, отражают ее основные функции. На основании концентрации альбумина оценивают процесс синтеза белка; уровни глюкозы и холестерина отражают роль печени в промежуточном метаболизме; а уровни желчных кислот и холестерина являются индикаторами проходимости желчевыводящих путей и кишечно-печеночной рециркуляции.
Печень поглощает, конъюгирует и выделяет билирубин, образующийся в результате расщепления гемоглобина фагоцитами. Метаболизация токсинов и лекарственных препаратов печенью может протекать незаметно, не вызывая биохимических изменений, или отражаться изменениями определенных сывороточных ферментов.
Лабораторные данные в рамках необходимого минимума собирают и обобщают, чтобы помочь выявить в печени четыре основных патологических процесса: гепатоцеллюлярное повреждение, холестаз, гепатоцеллюлярную дисфункцию/недостаточность, изменения кровообращения в системе воротной вены. Эти процессы часто происходят одновременно или являются следствием друг друга.
Однако существует также вероятность, что различные патологии могут оказывать на определенные анализируемые вещества противоположное воздействие, снижая их диагностическую чувствительность при патологии печени — например, уровень холестерина у собаки с тяжелым циррозом печени может находиться в пределах референсного интервала из‑за структурного холестаза, противодействующего снижению синтеза холестерина вследствие уменьшения массы печени (т. е. недостаточного количества гепатоцитов для выведения желчных кислот). Процесс-ориентированный подход облегчает целенаправленный отбор диагностических тестов и составление более четкого списка дифференциальных диагнозов.
Повреждение — довольно расплывчатый, но широко используемый термин, обозначающий негативное воздействие, которое в конечном счете приводит к нарушению проницаемости мембран гепатоцитов _ и, предположительно, к разной степени лизиса и гибели клеток. Печень может быть повреждена непосредственно из‑за воспаления паренхимы (первичный гепатит), токсинов (из лекарств и растений), опухоли (первичной или метастатической), в результате системного заболевания, нарушающего кровоток и доставку кислорода, либо эндокринопатии. Независимо от причины, для выявления повреждения этого типа используют всего несколько биохимических показателей.
Показатели «утечки» ферментов печени
Сывороточные ферменты, используемые для оценки состояния печени, подразделяют на две основные категории. Первая группа находится в цитозоле гепатоцитов, и ее появление в крови отражает «утечку» ферментов из гепатоцитов. У собак и кошек к этим ферментам относят аланинаминотрансферазу (АЛТ) и аспартатаминотрансферазу (АСТ). Повышение сыворотчной активности этих ферментов характерно для гепатоцеллюлярного повреждения, но только в том случае, если исключены гемолиз и тяжелое повреждение мышц (поскольку в мышечной ткани содержание АСТ выше, чем в печени) (5, 6).
Из‑за большого клеточного резерва печени и ее способности к регенерации величина повышения уровня этих ферментов пропорциональна количеству поврежденных гепатоцитов, но не отражает обратимость повреждения и не позволяет оценить синтетическую функцию печени (5, 7). Крайне важно оценивать показатели в динамике: период полужизни АЛТ у собак составляет 2–3 дня, у кошек — всего 3–4 часа, а период полужизни АСТ у собак составляет менее суток (5, 8).
Каждый биохимический анализ крови отражает состояние обмена веществ на определенный момент, поэтому при оценке клинической значимости изменений во времени необходимо учитывать период полужизни фермента. Важно помнить, что в печени при длительно протекающем невыраженном фиброзе может остаться мало жизнеспособных гепатоцитов, поэтому уровни активности АЛТ и АСТ в сыворотке крови могут быть минимально повышенными или даже находиться в пределах референсных значений, хотя заболевание на самом деле уже дошло до поздней стадии. Наибольшим увеличением «утечки» ферментов, как правило, сопровождаются поражения, связанные с воспалением или некрозом.
Воспалительные процессы в печени могут протекать скрыто. В ходе одного исследования лабрадор-ретриверов, у которых в первой линии родства были собаки с медь-ассоциированной гепатопатией, у 64% (122 из 191) клинически здоровых собак были обнаружены гистологические признаки воспалительного инфильтрата. Активность сывороточных ферментов в этой популяции оказалась относительно нечувствительным показателем как острого, так и хронического гепатита (9).
В отдельном исследовании при анализе 4559 биоптатов печени собак был выявлен повышенный уровень меди > 400 ppm по сухому весу (референсный диапазон 120–400) в 50% биоптатов, а в 19% биоптатов содержание меди оказалось > 1000 ppm. В том же исследовании предиктором уровня меди оказалось некровоспаление (т. е. иммунный ответ печени на некроз) (10). Накопление меди в печени кошек исследовано менее подробно, но у этого вида животных оно также вызывает гепатит (11).
Широко известной причиной умеренного повышения уровня АЛТ у кошек является гипертиреоз, но механизм этого явления не изучен (12). Глутаматдегидрогеназа (GLDH) и сорбитолдегидрогеназа (SDH) позволяют оценить «утечку» ферментов из гепатоцитов у других видов животных, однако их диагностическую ценность у кошек оценивали в небольшом количестве исследований по сравнению с собаками.
Индуцируемые ферменты
Второй набор ферментов, используемых для оценки состояния печени, называют индуцируемыми ферментами; к ним относятся щелочная фосфатаза (ЩФ) и гамма-глутамилтрансфераза (ГГТ). Гепатоциты усиливают синтез белков, которые продуцируют эти ферменты, вторично по отношению к так называемому индуктивному фактору — как правило, воздействию лекарств или гормонов (13).
Желчные кислоты тоже могут индуцировать эти ферменты, а также растворять клеточные мембраны; поэтому повышение ЩФ и ГГТ тесно связано с холестазом (14). Желчные канальцы реагируют на повышенное давление гиперплазией и увеличением количества клеток, продуцирующих ГГТ (15).
Поэтому при обструктивных холестатических процессах уровень ГГТ часто повышается значительнее, чем уровень ЩФ. Устойчивое повышение и ГГТ, и ЩФ может свидетельствовать о репарации и гиперплазии желчевыводящих путей. Как и при «утечке» ферментов, необходима оценка показателей в динамике. И у собак, и у кошек кости могут быть дополнительным источником ЩФ, поэтому при лабораторной оценке состояния печени необходимо учитывать заболевания, сопровождающиеся усиленным разрастанием костей, и возраст животного.
У собак этот фермент индуцируют кортикостероиды, поэтому у этого вида также учитывают воздействие эндогенных или экзогенных кортикостероидов (16). У кошек уровень ЩФ также повышается при гипертиреозе (17). У собак повышение АЛТ, ЩФ и ГГТ может развиться вследствие лечения фенобарбиталом (18). Если результаты лабораторных исследований неоднозначные, для установления диагноза можно использовать левамизол для подавления изофермента, индуцируемого кортикостероидами, но это требуется редко.
Индуцируемые ферменты могут высвобождаться из интактных гепатоцитов, но они высвобождаются также и при лизисе гепатоцитов. В таких случаях обычно ожидается значительное увеличение количества ферментов, выделяющихся из печени. Конечно, если лизису предшествовало индуктивное воздействие, картина уровня сывороточных ферментов может оказаться довольно запутанной.
Холестаз — это прекращение или снижение оттока желчи. Его могут вызвать уменьшение секреции желчи гепатоцитами или структурные повреждения на любом участке желчевыводящих путей, от мелких канальцев до желчного пузыря. Выведение желчи из гепатоцитов через эпителиальные клетки желчевыводящих путей и до просвета желудочно-кишечного тракта требует значительного расхода энергии, участия нескольких активных переносчиков и наличия осмотического градиента.
Таким образом, к холестазу могут привести сразу несколько потенциальных нарушений на различных этапах этого процесса (14).
Частые причины холестаза: увеличение размера гепатоцитов (например, при липидозе печени), опухолевые процессы, хроническое воспаление (фиброз), желчекаменная болезнь (холелитиаз), паразиты, панкреатит, киста слизистой желчного пузыря; а также факторы, вызывающие функциональный холестаз, такие как гипоксия и цитокин-опосредованное подавление экскреции.
Компрессионные поражения печени могут проявляться диффузно (например, у кошек липидоз печени вызывает увеличение гепатоцитов, сдавливающих желчные канальцы) или в виде объемного образования с поражением желчного пузыря или более крупных желчных протоков. Компрессионные поражения обычно сопровождаются накоплением других веществ, в выведении которых участвует система желчевыводящих путей. Поэтому многие структурные холестатические поражения проявляются гиперхолестеринемией и гипербилирубинемией.
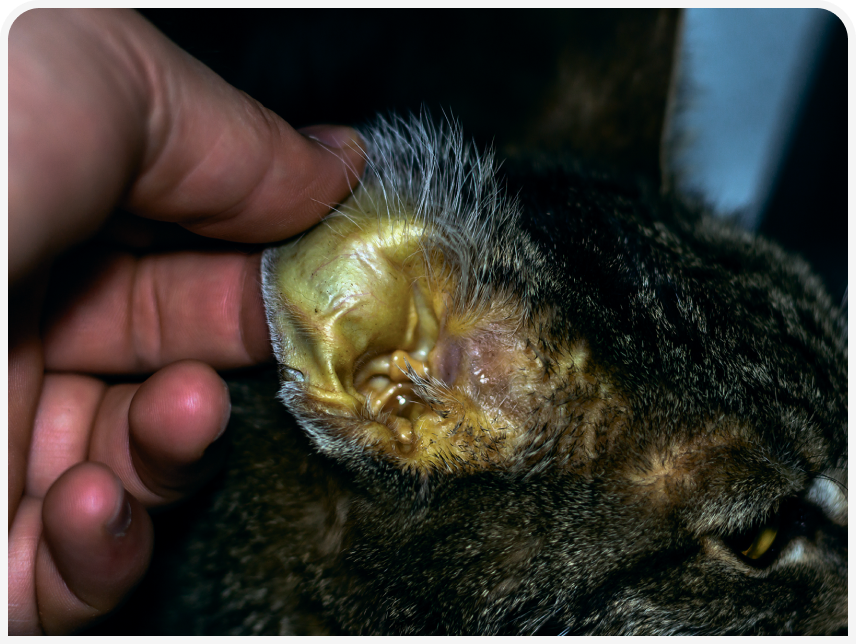
Желтуха, видимое пожелтение кожи, слизистых оболочек и склер из‑за накопления билирубина, — явный клинический признак возможного заболевания печени (Рисунок 1). Она развивается при гипербилирубинемии (Рисунок 2), обычно более 2–3 мг/дл (34–51 мкмоль/л).
Важно понимать, что отсутствие у животного желтухи не означает, что у него нет значимого поражения печени. Билирубин вырабатывается при расщеплении и переработке компонентов стареющих эритроцитов, и этот процесс происходит в два основных этапа.
Во-первых, эритроциты поглощаются и перевариваются макрофагами, а молекула гемоглобина ферментативно превращается в билирубин. Эта стадия обычно происходит в макрофагах селезенки и в меньшей степени в клетках Купфера (макрофагах печени).
Во-вторых, выработанный макрофагами неконъюгированный билирубин нековалентно связывается с альбумином и переносится в печень, где поглощается гепатоцитами и ферментативно конъюгируется для облегчения выведения с желчью. Гипербилирубинемия может возникнуть при гемолитическом процессе — гемолитической («надпеченочной») желтухе. Гемолиз ускоряет обмен эритроцитов и расщепление гемоглобина. В этих случаях печень просто перегружена, и в крови первоначально накапливается неконъюгированный билирубин (19).
При острой анемии в печени развивается гипоксия, снижающая запас энергии в гепатоцитах и замедляющая выведение билирубина. Подавляют выведение билирубина также и воспалительные цитокины. Таким образом, у животного с гемолитической анемией (надпеченочной желтухой) имеется вторичный печеночный компонент, который обусловлен биохимическими поражениями.
«Печеночную» или «постпеченочную» желтуху вызывают либо внутриклеточные биохимические поражения, либо структурные поражения c физическим препятствием выведению билирубина с желчью (например, холестаз). Печеночная и постпеченочная желтуха часто вызваны одними и теми же причинами.
При дифференциальной диагностике после исключения гемолитической (надпеченочной) желтухи задача сводится к определению того, есть ли биохимические нарушения в гепатоцитах и/или эпителиальных клетках желчных протоков, или же присутсвуют структурные повреждения (обычно определяются методами визуальной диагностики, а не лабораторными исследованиями).
Печень вырабатывает множество белков, больше всего — альбумина, но также белки острой фазы и несколько факторов свертывания крови. Кроме того, печень — основное место глюконеогенеза, синтеза холестерина и ферментов цикла образования мочевины. Таким образом, альбумин, глюкоза, холестерин и мочевина используются в сочетании, чтобы определить способность печени эффективно участвовать в промежуточном обмене веществ. Если у собаки или кошки недостаточно функционирующих гепатоцитов из‑за повреждения или атрофии, количество всех этих четырех анализируемых веществ может быть снижено. Однако на эти анализируемые вещества влияют и другие процессы.
Альбумин является «негативным» белком острой фазы воспаления и может выводиться из организма несколькими путями, включая мочевыделительную систему или желудочно-кишечный тракт, а также в результате кровотечения или экссудации. Исключить или подтвердить эти диагнозы можно по общим анализам крови и мочи.
Синтез холестерина снижается при мальабсорбции (нарушении всасывания в кишечнике), гипоадренокортицизме и некоторых видах рака, поэтому нарушение синтетической функции печени признают ведущей причиной снижения уровня холестерина, только когда исключены вышеперечисленные патологии (20–22). Методы визуальной диагностики позволяют оценить общий размер печени и выявить признаки фиброза.
Подозрение на нарушение кровотока и последующее снижение клиренса (показатель скорости очищения) в печени можно подтвердить, измерив уровень желчных кислот. Повышенное содержание желчных кислот в сыворотке крови может свидетельствовать о снижении массы гепатоцитов и/или портосистемном шунте (когда желчные кислоты остаются в системном кровотоке, поскольку кровь минует печень). Уровень желчных кислот, вероятно, будет повышен, если есть биохимические изменения, связанные с холестазом, что затрудняет использование этого теста для оценки массы печени и кровотока.
При сопутствующем заболевании подвздошной кишки нарушается всасывание желчных кислот, выделяемых в желудочно-кишечный тракт. Поэтому у животных с выраженными поражениями печени и нарушением всасывания в подвздошной кишке уровень желчных кислот может оставаться в пределах нормы. Динамическая проба с желчными кислотами (измерение до и после приема пищи) повышает чувствительность метода, хотя у 15–20% собак при исследовании натощак их уровень оказывается выше, предположительно из‑за задержки опорожнения желудка или спонтанного сокращения желчного пузыря. В этих случаях для интерпретации следует использовать большее из двух значений (23).
Аммиак, продукт белкового обмена, также выводится из организма печенью. В отличие от желчных кислот, в его клиренсе нет энтерогепатического компонента, поэтому холестаз на концентрацию аммиака в плазме крови не влияет. Этот метод может быть чувствительным и специфичным для оценки массы гепатоцитов и поступления крови в печень, но образцы крови при этом требуется получать и обрабатывать специальным образом (Блок 1).
Такой тест проводят не во всех лабораториях, поэтому перед направлением образца в лабораторию следует уточнить ее возможности.
У кошек тест на аммиак является более специфичным, но менее чувствительным методом, чем проба с желчными кислотами, для выявления шунта или уменьшения массы печени (24). Нарушения цикла выработки мочевины также могут вызывать гипераммониемию, но другие биохимические признаки патологии печени при этом обычно отсутствуют.
Почки собак имеют низкий почечный порог для конъюгированного билирубина, поэтому у них при холестазе билирубинурия часто может предшествовать гипербилирубинемии. При длительно протекающих холестатических заболеваниях конъюгированный билирубин может ковалентно связываться с альбумином, образуя дельта-билирубин.
Эта связь удерживает билирубин в крови, поэтому отсутствие билирубинурии у животного с другими признаками холестаза не позволяет исключить холестатический процесс.
Клетки почечных канальцев у кобелей могут конъюгировать некоторое количество билирубина, поэтому небольшое количество билирубина в моче у них может быть клинически незначимо. Мочевина необходима почкам для концентрирования мочи, поэтому снижение синтеза мочевины в печени может оказать на почки вторичное неблагоприятное воздействие.
У многих животных с заболеваниями печени концентрационная функция почек снижается, моча будет иметь низкий удельный вес, может развиться полиурия (Рисунок 3). У кошек при билирубинурии всегда требуется дообследование. Попадание аммиака в мочу может привести к образованию кристаллов биурата аммония.
Морфология эритроцитов
На морфологию эритроцитов могут влиять изменения уровня липопротеинов в сыворотке крови при заболеваниях печени. Это проявляется пойкилоцитозом, часто наблюдаемым у кошек с липидозом печени (Рисунок 4). При портосистемном шунте может наблюдаться микроцитоз, иногда — с анемией. Акантоциты слабо связаны с поражениями печени.
Печеночная коагулопатия
Печень вырабатывает не только факторы свертывания крови, но и ряд белков — ингибиторов свертывания крови, включая протеин С и протеин S. При снижении синтетической функции печени может наблюдаться склонность либо к кровотечениям, либо к тромбозам.
Желудочно-кишечные заболевания, при которых снижается уровень витамина К, препятствуют образованию в гепатоцитах факторов карбоксилирования, что может привести к нарушению свертывания крови. Период полужизни фактора VII самый короткий, поэтому в этих случаях протромбиновое время может увеличиться прежде активированного частичного тромбопластинового времени.
Протеин С и СРБ
Протеин С и С-реактивный белок (СРБ, CRP), вырабатываются в печени и оба могут быть точно измерены у домашних животных. Однако досадное сходство в номенклатуре может привести к случайной ошибке при выборе метода исследования.
Доказано, что протеин С отражает синтетическую функцию печени и гепатопортальную перфузию; это компонент с основным антикоагулянтным действием, поэтому по его концентрации в сыворотке крови выявляют портосистемные шунты и дисплазию микрососудов (поскольку у собак с шунтами его концентрация стабильно снижена).
Повышение концентрации протеина С также позволяет следить за эффективностью лигирования портосистемного шунта в динамике. Анализ на протеин С оценивает его активность в крови с использованием цитратированной плазмы; С-реактивный белок (СРБ) может быть измерен в сыворотке или плазме крови, в зависимости от используемого метода.
Выпот в брюшную полость
Гипоальбуминемия может способствовать снижению онкотического давления в крови, а фиброзные изменения в печени могут повышать давление в ее сосудистой сети и синусоидах. Поэтому у животного с значительной патологией печени может наблюдаться выпот в брюшную полость (Рисунок 5), чаще всего транссудативный.
При подозрении на заболевания печени у домашних животных важно помнить, что системные процессы могут приводить к развитию вторичного поражения печени, поэтому ветеринарному врачу следует отдельно рассмотреть признаки повреждения печени или холестаза, чтобы определить преобладающую причину.
Полезно осуществить поиск признаков нарушения синтетической функции печени по уровням глюкозы, мочевины, холестерина и альбумина, а также обязательно провести общий анализ крови и мочи.
Самое главное: поскольку биохимический анализ крови отражает состояние обмена веществ на момент получения образца, в большинстве случаев решающее значение имеет оценка показателей в динамике. Выявление повреждения печени

Холестаз
.png)
Гипербилирубинемия и желтуха
.png)
Синтетическая функция печени и портальное кровообращение

Полезная информация, которую можно получить из анализа мочи
.png)
Дополнительные данные по методам исследования
.png)
.png)
Заключение
«Лабораторная оценка функции печени »!
баллы


были начислены ранее


телефона ниже для сброса пароля.



на номер
+7 {{ formatted_phone }}


Вы успешно прошли тест!
зарегистрироваться/авторизоваться
способ авторизации/регистрации.
{{ formatted_phone }}.
Введите последние четыре цифры номера входящего звонка.

весь модуль
всех видеоуроков модуля














 18
18  10 мин
10 мин







.jpg)