Введение
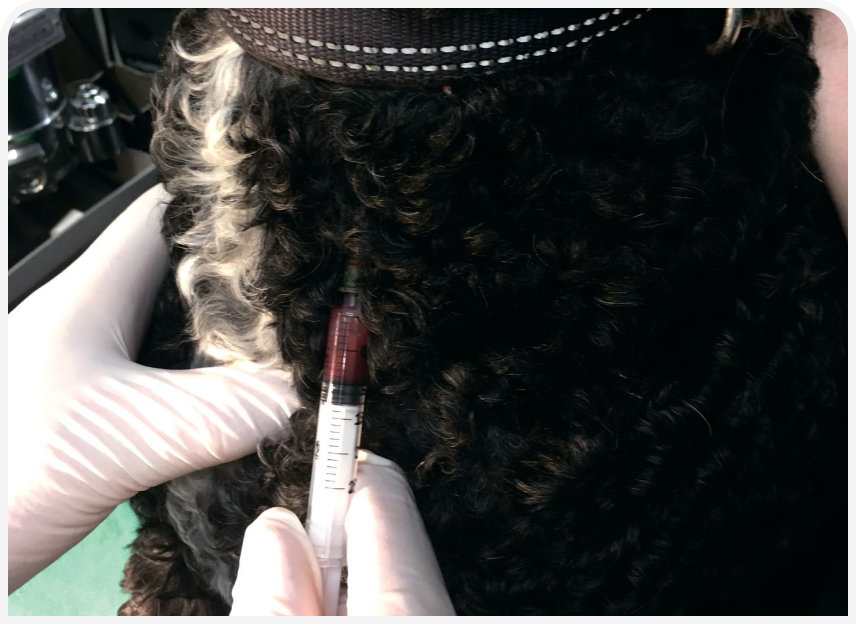
Большинство ветеринарных врачей, работающих с мелкими домашними животными, несколько раз в день получают образцы крови при обследовании своих пациентов (Рисунок 1). Однако интерпретация результатов не всегда бывает однозначной, особенно в отношении параметров функции печени, и полезно знать, какие исследования представляют наибольшую ценность для диагностики и мониторинга определенных клинических состояний. В статье рассмотрены ответы на некоторые наиболее частые вопросы относительно печеночных ферментов.
Когда высокий уровень АЛТ/АСТ/ЩФ клинически значим?
Как правило, значимым считают двукратное повышение уровней аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ). С точки зрения патофизиологии, повышенная активность гепатоцеллюлярных ферментов вызвана утечкой (АЛТ, АСТ) или индукцией синтеза (щелочная фосфатаза — ЩФ) ферментов.
Однако результаты анализов всегда следует интерпретировать в свете истории болезни пациента, клинических проявлений и дополнительных диагностических данных; например, при остром или хроническом течении заболевания результаты могут различаться. Хроническое заболевание может сопровождаться атрофией или фиброзом печени, и тогда активность печеночных ферментов может находиться в пределах референсного интервала или повышаться незначительно.
Поскольку при тяжелом течении заболевания функция печени может быть нарушена, нормальные уровни печеночных ферментов в сочетании с изменениями параметров функции печени (например, развиваются гипоальбуминемия, гипербилирубинемия, гипогликемия, снижается содержание азота мочевины в крови (АМК), изменяются концентрации холестерина и триглицеридов, увеличивается время свертывания крови) соответствуют классической картине тяжелого заболевания, такого как портосистемный шунт.
Таким образом, вывод, что нормальная активность печеночных ферментов свидетельствует о здоровой печени, явно неверен. При интерпретации результатов определения печеночных ферментов всегда необходимо одновременно оценивать параметры функции печени и соотносить их с анамнезом и клиническими проявлениями у пациента.
Какие лабораторные тесты позволяют лучше всего диагностировать портосистемный шунт?
Портосистемный шунт — это аномальное строение сосудов, при котором вена портальной системы напрямую соединяется либо с каудальной полой веной, либо с непарной веной. Из‑за этого к гепатоцитам поступает недостаточно крови, что приводит к атрофии и уменьшению размеров печени.
Потеря гепатоцитов может сопровождаться самыми разнообразными лабораторными изменениями. Уровни печеночных ферментов, таких как цитозольные ферменты АЛТ или АСТ, преимущественно содержащихся в митохондриях гепатоцитов, у этих пациентов могут быть нормальными или повышенными. Однако если количество гепатоцитов уменьшилось существенно, оставшиеся клетки могут не выделять значительного количества этих ферментов, что приводит к нормальным или сниженным показателям их концентрации в сыворотке крови. Когда от массы печени остается только 20–30%, проявляются симптомы печеночной недостаточности.
В таких случаях печень больше не может поддерживать физиологические функции, вследствие чего изменяется углеводный, липидный, витаминный и белковый обмен, а также нарушается способность печени к детоксикации. В результате недостаточности могут развиваться гипогликемия, изменение концентрации холестерина и триглицеридов, гипербилирубинемия, гипоальбуминемия, увеличение времени свертывания крови, снижение концентрации мочевины, повышение уровня желчных кислот и/или гипераммониемия. Наряду с этими изменениями часто можно наблюдать микроцитарную анемию и снижение удельного веса мочи.
Итак, какой анализ лучше всего использовать при подозрении на портосистемный шунт, если вышеупомянутые тесты не позволяют четко установить диагноз? При печеночной недостаточности большое значение имеет оценка уровня желчных кислот натощак и после приема пищи / пищевой стимуляции.
Обратите внимание, что на фоне гипербилирубинемии следует ожидать повышения концентрации желчных кислот, и тест с желчными кислотами может не дать дополнительной информации. Механизм заключается в том, что заболевания, приводящие к нарушению выделения конъюгированного билирубина из гепатоцитов в желчные канальцы, также нарушают выведение желчных кислот и вызывают повышение их концентрации в крови.
При наличии неврологических признаков, указывающих на печеночную энцефалопатию (например, ступора или тремора), наиболее полезно оценить уровень аммиака. Однако этот параметр очень чувствительный, и неправильное обращение с образцами может легко привести к ложноповышенным результатам. Чтобы ограничить вариабельность результатов и снизить риск ложного диагноза, очень важно немедленно центрифугировать образец и отделить клетки от плазмы, провести измерение в течение одного часа после получения образца и ограничить его контакт с воздухом.
Такое возможно! Чтобы понять механизмы, приводящие к повышению активности ферментов, полезно вернуться к патофизиологии. Группа печеночных ферментов неоднородная; как правило, АЛТ и АСТ рассматриваются как «печеночные ферменты», а ЩФ и гамма-глутамилтрансфераза (ГГТ), хотя их часто и включают в эту категорию, образуются в мембране эпителиальных клеток желчевыводящих путей и поэтому являются классическими маркерами внутри- или внепеченочных холестатических нарушений.
Активность АЛТ и АСТ повышается вследствие обратимого или необратимого (некроз) повреждения гепатоцитов. Печень могут поражать самые разные опухоли; первичное новообразование в печени может быть очаговым или узловым (например, большинство гепатоцеллюлярных карцином) или расти диффузно, рассеиваясь в печеночной ткани. Из‑за тяжелой деструкции гепатоцитов и некроза тканей очаговые поражения могут вызвать значительное повышение активности печеночных ферментов. В зависимости от степени внутрипеченочного холестаза уровень ЩФ может быть нормальным или повышенным. Диффузная инфильтрация ткани печени круглоклеточными опухолями (например, лимфомой или мастоцитомой) может не сопровождаться значимым поражением гепатоцитов, и в таких случаях активность печеночных ферментов может повышаться незначительно или вообще оставаться нормальной.
Таким образом, любое общее повышение активности печеночных ферментов при новообразованиях в печени определяется степенью повреждения гепатоцитов и последующим высвобождением ферментов и/или степенью связанного с поражением опухолью некроза тканей.
Очаговое или диффузное новообразование в печени не всегда будет приводить к повышению уровня печеночных ферментов, поэтому для выявления заболевания печени важно дополнительно провести УЗИ брюшной полости и тонкоигольную аспирационную биопсию (Рисунок 2).
Поскольку печень в организме выполняет центральную регулирующую функцию для многих метаболических процессов, вторичные гепатопатии встречаются часто. Например:
Холестаз, как внутри-, так и внепеченочный, обычно приводит к повышению активности печеночных ферментов. Благодаря физиологическому расположению в клетках желчного эпителия ферменты ЩФ и ГГТ позволяют с высокой чувствительностью выявлять это состояние. Внутрипеченочный холестаз в результате отека гепатоцитов и последующей обструкции желчных канальцев может наблюдаться при гепатите любой этиологии.
При таких заболеваниях также часто повышаются уровни ферментов АЛТ и АСТ. Внепеченочный холестаз развивается в результате состояний, при которых возникает обструкция желчных протоков. К ним относятся воспаление, новообразования, холелитиаз. Из‑за близкого расположения печени к поджелудочной железе панкреатит может приводить к развитию внепеченочного холестаза, и в таких случаях полезно оценить уровень липазы DGGR (сложный эфир 1,2-о-дилаурил-рак-глицеро-3-глутаровой кислоты с 6-метилрезоруфином).
Системные заболевания, которые могут оказывать влияние на печень, многочисленны, и в их число входят воспалительные состояния, такие как желудочно-кишечные заболевания, панкреатит и сепсис. Из кишечника всасываются через воротную вену и поступают в печень не только нутриенты, минеральные вещества, микроэлементы и витамины; при желудочно-кишечных заболеваниях переносятся также бактерии, токсины, лекарственные препараты и/или цитокины.
Связанные с этим цитологические изменения в гепатоцитах заключаются в накоплении жидкости и/или гликогена и обычно выражены слабо. Следовательно, активность АЛТ повышается обычно также незначительно. Инфекционные заболевания, включая бактериальные (например, лептоспироз), вирусные (например, аденовирусная инфекция собак 1 типа) или грибковые (например, гистоплазмоз), могут сопровождаться значительным повышением уровня печеночных ферментов.
Для печени жизненно важно снабжение кислородом, поэтому гипоксия на фоне анемии, гемолиза или сердечно-сосудистых заболеваний может привести к повреждению гепатоцитов и повышению активности печеночных ферментов.
Повреждение мышц также следует учитывать; активность фермента АСТ неспецифична для печени, она также может повышаться после повреждения мышц из‑за его локализации в сердечной и скелетной мышечной ткани. Из‑за неспецифичности уровень АСТ полезно оценивать в сочетании с другими лабораторными параметрами. АЛТ может также повышаться при некоторых редких мышечных дистрофиях; активные мышечные заболевания в большинстве случаев не сопровождаются утечкой АЛТ.
Таким образом, при одновременном повышении уровня АЛТ происхождение ферментов, скорее всего, печеночное. Если в анамнезе пациента имеются данные о возможной травме или воспалении мышц, измерение активности фермента креатинкиназы (КК) может помочь установить, что причиной повышения уровня АСТ является заболевание мышц.
Гемолиз эритроцитов может привести к незначительному повышению активности АСТ, поскольку этот фермент также присутствует в эритроцитах. Этот пример показывает, что гематологические данные крайне важно оценивать вместе с биохимическими.
Интоксикации, в частности прием лекарственных препаратов, часто вызывают повышение уровня печеночных ферментов. Наиболее важным механизмом является индукция выработки ферментов этими веществами, и это одна из основных причин повышения активности ЩФ. Такое действие описано у антиконвульсантов фенобарбитала и примидона. Также необходимо упомянуть глюкокортикоиды (особенно преднизолон и преднизон), поскольку на активность ЩФ могут повлиять даже мази для местного применения (Рисунок 3).
Первостепенное значение здесь имеет тщательный анализ истории болезни пациента, поскольку владельцы могут не осознавать влияние таких лекарств и упоминать о них только после того, как их специально спросят.
Глюкокортикоиды стимулируют выработку специфичной для собак индуцируемой кортикоидами изоформы ЩФ (C-ALP). Повышение активности ЩФ может наблюдаться в течение семи дней после начала лечения, а снижение — только через шесть недель после прекращения терапии. Интерпретация ответа активности ЩФ на лечение еще более усложняется, поскольку изменения уровня фермента зависят от типа, дозы, продолжительности лечения и способа введения (перорально, внутривенно или местно) применяемого стероида. Дополнительно усложняет интерпретацию непредсказуемый характер реакции на определенные виды лечения у некоторых пациентов.
Состояние костей также может влиять на активность печеночных ферментов, поскольку ЩФ существует в различных изоформах. Костная изоформа ЩФ образуется в остеобластах, поэтому у молодых растущих животных может наблюдаться увеличение ее содержания вплоть до трехкратного уровня из‑за повышенной активности остеобластов.
Остеосаркома может сопровождаться усиленным ремоделированием кости; поэтому при повышении уровня ЩФ у взрослых пациентов одним из дифференциальных диагнозов является костное новообразование (Рисунок 4). Следует также учитывать другие заболевания костей (например, некроз, переломы и ортопедические вмешательства).
Эндокринопатии зачастую также приводят к повышению активности печеночных ферментов. Высокие уровни эндогенных глюкокортикоидов, например при гиперадренокортицизме (болезни Кушинга), индуцируют активность изоформы C-ALP, что является характерным признаком этого заболевания.
Если уровень этого фермента не повышен, болезнь Кушинга менее вероятна, но диагноз все равно основывается на соответствии клинических признаков, данных лабораторных исследований и результатов специальных тестов, таких как малая дексаметазоновая проба. Другие эндокринные заболевания, такие как гиперпаратиреоз и сахарный диабет, тоже могут потенциально вызвать повышение уровня печеночных ферментов.
Краеугольный камень мониторинга сахарного диабета — оценка уровня глюкозы. Однако при сахарном диабете нарушается липидный обмен и затем активируется метаболизация липидов в печени, поэтому мониторинг печеночных ферментов позволяет оценивать течение заболевания. При цитологическом исследовании может наблюдаться стеатоз печени, хотя у кошек он более выражен, чем у собак. Накопление липидов в гепатоцитах приводит к их повреждению и может сопровождаться повышением уровня АЛТ или ЩФ (последний фермент в качестве маркера липидоза печени у кошек особенно чувствителен), а в образце крови можно обнаружить выраженную липемию (Рисунок 5).
Как упоминалось выше, противосудорожные препараты, такие как фенобарбитал, могут индуцировать выработку фермента ЩФ. Во время терапии важно оценивать уровень фенобарбитала, так как дозировка препарата > 35 мкг/мл гепатотоксична, и поэтому собаке, постоянно получающей фенобарбитал, рекомендуется проводить мониторинг общего состояния печени два раза в год.
Как отмечено выше, уровни печеночных ферментов в пределах референсного интервала не исключают значимой печеночной недостаточности, поэтому при подозрении на нарушение функции печени у собаки, получающей противосудорожную терапию, следует рассмотреть возможность провести динамическую пробу c желчными кислотами.
Печень вырабатывает не только факторы свертывания крови, но и белки-антикоагулянты, такие как протеин S и протеин С, антитромбин и плазминоген. Таким образом, изменения функции печени приводят к снижению выработки и функции про- и антикоагулянтных белков, и развивается клиническая картина коагулопатии, от тяжелой (например, спонтанного кровотечения) до субклинической (увеличение времени свертывания крови).
Реакцию у отдельного пациента предсказать трудно. Как правило, для существенного нарушения синтеза описанных факторов и белков необходимы значительное снижение массы печени и последующее развитие тяжелой печеночной недостаточности. Поскольку самый короткий период полувыведения из всех факторов свертывания крови имеет фактор VII (6 часов), ожидается, что вначале изменится протромбиновое время (ПВ).
Во многих случаях при подозрении на гепатопатию для уточнения характера заболевания требуется тонкоигольная аспирационная или пункционная биопсия печени, но у пациентов с печеночной недостаточностью перед получением биоптата оценивают риск, для чего проводят оценку показателей свертываемости крови, таких как ПВ и активированное частичное тромбопластиновое время (аЧТВ), хотя корреляция между этими факторами с риском развития кровотечений непрямая.
Значительное увеличение времени свертывания может сопровождаться спонтанным кровотечением или кровотечением при биопсии, но иногда кровотечение развивается и при незначительном увеличении или даже нормальном времени свертывания крови.
Динамическая проба с желчными кислотами — наиболее чувствительный метод оценки уровня желчных кислот для диагностики печеночной недостаточности. Измеряют уровень желчных кислот натощак (обычно после 12-часового голодания) и сравнивают эти исходные данные с образцом, полученным через 2 часа после приема пищи с умеренным содержанием жиров. Потребление пищи стимулирует сокращение желчного пузыря и выделение желчных кислот в кишечно-печеночную циркуляцию.
Поскольку исходное время сокращения желчного пузыря неизвестно при получении первичного результата, прием пищи, скорее всего, его стимулирует, поэтому оценить функцию печени становится легче.
Интерпретировать результаты этой пробы может оказаться сложно, поскольку необходимо обеспечить контролируемый прием пищи и исключить желудочно-кишечные заболевания, задерживающие опорожнение желудка или снижающие всасывание желчи в подвздошной кишке. Момент сокращения желчного пузыря непредсказуем, и накопленная желчь может выделиться не полностью или желчный пузырь может наполниться желчью не полностью, что также может повлиять на результаты. На кишечно-печеночную циркуляцию желчных кислот также влияет метаболизм кишечных бактерий.
Общее эмпирическое правило при интерпретации результатов — оценивать наибольшее полученное значение, будь то исходное или после стимуляции. Если в обоих образцах содержание желчных кислот превышает 25 мкмоль/л, это подтверждает печеночную недостаточность. Уровень желчных кислот натощак также может быть повышен при холестазе или других вторичных гепатопатиях. Значения > 50 мкмоль/л позволяют в первую очередь подозревать первичные гепатопатии.
Результаты определения уровня желчных кислот до и после приема пищи в диапазоне 20–50 мкмоль/л неоднозначные, поэтому требуются повторный анализ через 2–3 недели и сопоставление с другими лабораторными данными и/или результатами инструментальных методов диагностики. Наконец, следует отметить, что аномальные значения содержания желчных кислот могут быть следствием различных сопутствующих заболеваний гепатобилиарной системы и не являются специфичными.
Учитывая, что практически всегда при биохимическом анализе крови у собаки анализируют множество параметров, которые могут быть использованы для оценки функции печени, важно знать, когда аномальный результат следует считать значимым, а когда даже результат в пределах референсного интервала не позволяет исключить потенциальный диагноз. Врачу рекомендуется всегда интерпретировать результаты исследования печеночных ферментов с учетом истории болезни пациента и клинических проявлений, при необходимости повторять определенные анализы и искать дополнительные варианты диагностики. Почему у собаки с первичной опухолью печени уровень печеночных ферментов может быть нормальным?
.png)
Какие заболевания, не связанные с печенью, могут значимо влиять на ферменты печени?
.png)
.png)
Насколько полезно определение печеночных ферментов при мониторинге сахарного диабета?
.png)
Какие анализы следует назначать собаке, длительное время получающей антиконвульсанты?
Нужно ли исследовать факторы свертывания крови у собаки с заболеванием печени?
Нужно ли исследовать факторы свертывания крови у собаки с заболеванием печени?

Заключение
«Распространенные вопросы о ферментах печени у собак»!
баллы


были начислены ранее


телефона ниже для сброса пароля.



на номер
+7 {{ formatted_phone }}


Вы успешно прошли тест!
зарегистрироваться/авторизоваться
способ авторизации/регистрации.
{{ formatted_phone }}.
Введите последние четыре цифры номера входящего звонка.

весь модуль
всех видеоуроков модуля














 242
242  10 мин
10 мин







.jpg)